
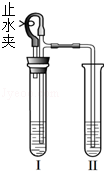
用如图所示装置分别进行两个实验(已知:氯化钙溶液呈中性).
(1)打开止水夹,向Ⅰ中液体加入一种黑色固体、Ⅱ中液体加入一种白色固体.Ⅰ和Ⅱ中均有气泡出现,且Ⅱ中液体内出现燃烧现象.
①写出燃烧反应的化学方程式 .
②请说明Ⅱ中出现燃烧的原因 .
(2)打开止水夹,向Ⅰ中液体加入一小块固体.Ⅰ和Ⅱ中均有气泡出现,且Ⅱ中液体出现浑浊现象.关闭止水夹,发现Ⅱ中液面上升,溶液由浑浊变澄清.
①请说明溶液由浑浊变澄清的原因 .
②若实验后Ⅱ中澄清液中的溶质由一种或两种物质组成,为检验其成分,应该进行的实验操作是
.
(1)①4P+5O2 2P2O5;②白色固体是可燃物,与氧气接触并达到着火点;
2P2O5;②白色固体是可燃物,与氧气接触并达到着火点;
(2)①Ⅰ中盐酸进入Ⅱ中将碳酸钙完全反应;②取Ⅱ中的澄清液于试管中,向其中滴加紫色石蕊溶液.
解析试题分析:(1)①Ⅱ中液体内出现燃烧现象,说明白色固体是可燃物,与氧气接触并达到着火点,因此白色固体的着火点很低,是白磷,白磷燃烧的化学方程式是4P+5O2 2P2O5;②Ⅱ中液体内出现燃烧现象,说明白色固体是可燃物,与氧气接触并达到着火点;(2))①Ⅱ中导管口有气泡冒出,溶液浑浊,可知产生的气体为二氧化碳,溶液浑浊的反应是CO2+Ca(OH)2=CaCO3↓+H2O,因此Ⅰ中产生二氧化碳的反应是CaCO3+2HCl═CaCl2+H2O+CO2↑;关闭止水夹,Ⅰ中不断生成的二氧化碳使装置内的气压变大,因此Ⅰ中盐酸进入Ⅱ中将生成的碳酸钙完全反应掉,因此溶液由浑浊变澄清;②实验后Ⅱ中澄清液中一定有氯化钙,氯化钙溶液显中性;若盐酸过量,盐酸将氢氧化钙反应掉后有剩余,因此还会有氯化氢,盐酸显酸性;若盐酸不足,溶液中会有氢氧化钙,氢氧化钙溶液显碱性,所以为检验其成分,应该进行的实验操作是取Ⅱ中的澄清液于试管中,向其中滴加紫色石蕊溶液.
2P2O5;②Ⅱ中液体内出现燃烧现象,说明白色固体是可燃物,与氧气接触并达到着火点;(2))①Ⅱ中导管口有气泡冒出,溶液浑浊,可知产生的气体为二氧化碳,溶液浑浊的反应是CO2+Ca(OH)2=CaCO3↓+H2O,因此Ⅰ中产生二氧化碳的反应是CaCO3+2HCl═CaCl2+H2O+CO2↑;关闭止水夹,Ⅰ中不断生成的二氧化碳使装置内的气压变大,因此Ⅰ中盐酸进入Ⅱ中将生成的碳酸钙完全反应掉,因此溶液由浑浊变澄清;②实验后Ⅱ中澄清液中一定有氯化钙,氯化钙溶液显中性;若盐酸过量,盐酸将氢氧化钙反应掉后有剩余,因此还会有氯化氢,盐酸显酸性;若盐酸不足,溶液中会有氢氧化钙,氢氧化钙溶液显碱性,所以为检验其成分,应该进行的实验操作是取Ⅱ中的澄清液于试管中,向其中滴加紫色石蕊溶液.
考点:反应现象和本质的联系.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:初中化学 来源: 题型:探究题
酸、碱、盐是几类有广泛用途的重要化合物.
(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是 (提示:只有其中一种).
②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 | 白色沉淀全部溶解,并产生大量气泡 |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
老师请化学兴趣小组的同学帮助他将失去标签的碳酸钠、稀盐酸、氯化钠、氢氧化钠和氯化钙溶液鉴别出来.重新贴好标签.为了区分这五种溶液,将试剂瓶编号为A,B,C,D,E,该小组同学进行了如下探究:
| | 实验步骤 | 实验现象 | 实验结论 |
| 步骤一 | 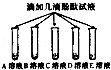 | B,C溶液呈现红色 A,D,E溶液颜色无明显变化 | B,C溶液显 性 |
| 步骤二 | 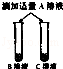 | B,C溶液红色均消失, 且C溶液中产生大量气泡 | 可确定B为 溶液;A与C的反应通常 不用作实验室制取气体的 原因是 |
| 步骤三 |  | E中无明显现象, D中的现象为 | 确定E为氯化钠溶液, 则D溶液与所加试剂发生反应的化学方程式为 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| 1 | 5 | 1 | 20 | 0.1 | 4 | 16.74 |
| 2 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| 3 | 30 | 5 | 35 | | 2 | 49.21 |
| 4 | 30 | 5 | 55 | | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题。
Ⅰ.结构:
NaOH含有钠元素,钠在元素周期表中处于第三周期的 (填“开头”、“中间”或“结尾”)。
NaOH属于碱,碱在溶液中都可以电离出相同的离子,该离子是 (填离子符号)。
Ⅱ.制备:
实验室用纯碱制备烧碱的化学反应方程式为 。Ⅲ.性质及变化:
(1)氢氧化钠固体曝露在空气中容易 ,因此它与生石灰一起用作某些气体的干燥剂
(2)如右图所示,NaOH溶液可与稀酸反应的方程式为 。
该反应没有明显的现象,为了说明该反应确实能够发生,下列哪种物质肯定无法帮助你达到目的 。
a.镁条 b.酚酞 c.CuSO4 d.Ba(NO3)2
Ⅳ.保存:
张老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH固体,他让同学们对这瓶NaOH固体进行探究
【提出猜想】
猜想I:没有变质
猜想Ⅱ:部分变质为Na2CO3,依据是 (用方程式表示);猜想Ⅲ:全部变质
【实验设计、现象和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某班多个化学兴趣小组,在学习碱的化学性质时,进行了如图1所示的实验.
(1)小明组反应后A中溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ;小红组做完A实验后溶液呈无色,用微观理论解释变无色的反应的实质 .
(2)小红组做B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K1、K2均处于关闭状态).B实验全过程的操作及现象 .请写出氢氧化钠与二氧化碳反应的化学方程式 .
(3)实验结束后,小军将以上同学做的A、B两个实验的废液均倒入同一个大烧杯中,观察到混合后的废液呈红色,由此产生疑问.
[提出问题]大烧杯的废液中含有哪些溶质?(酚酞除外)
[查阅资料]氯化钙溶液呈中性,CaCl2+Na2CO3=CaCO3↓+2NaCl
[实验验证]取一定量的废液,逐滴加入氯化钙溶液,如图2为同学们根据部分实验现象绘制的关系曲线.
[实验结论]如果观察到的现象只有沉淀产生,溶液仍然为红色,则废液中的溶质为 ;
如果观察到 ,则废液中的溶质为 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
Y型管是实验改进时经常使用的仪器.
(1)用图1所示装置研究可燃物燃烧的条件.已知:白磷的着火点为40℃,红磷的着火点为240℃.
①若在a处放置红磷,在Y型管中可以观察到的现象是 .
②若要研究可燃物燃烧的另一个条件,应在a处加入 .
(2)用图2所示装置可以研究二氧化碳的相关性质.
①在不打开装置的情况下,将Y型管I向右倾斜,使稀硫酸流入碳酸钠中,再恢复至图示装置的角度,即可产生二氧化碳.Y型管II中的现象是 .
②不改换实验仪器,将上述实验进行修改,即可证明二氧化碳的密度大于空气密度.修改方法是 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某兴趣小组在实验台上发现一瓶标签部分破损、未盖瓶塞的溶液(如图),于是同学们决定利用实验台上的其他药品对这瓶溶液进行实验探究:
[提出问题]这瓶溶液是什么溶液?(不考虑碳酸氢钠)
[提出猜想]这瓶溶液是:
猜想一:氯化钠溶液;
猜想二:氢氧化钠溶液;
猜想三:碳酸钠溶液:
猜想四:硫酸钠溶液.
[实验推断]
(1)小香取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是氯化钠溶液,也不可能是硫酸钠溶液,理由是 ;(2)小芳另取样滴加稀盐酸,观察到有 产生,得出结论;该溶液是碳酸钠溶液.
(3)小美认为小芳的结论不完全正确,理由是
小组同学讨论后一致认为还需要进行如下实验:
[继续探究]另取样,加入 溶液,观察到有白色沉淀产生,再取上层清液,滴入酚酞试液,溶液呈红色.
[实验结论]由此推测出这瓶溶液最初是 溶液(写化学式),敞口放置过程中发生了变化,反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com