
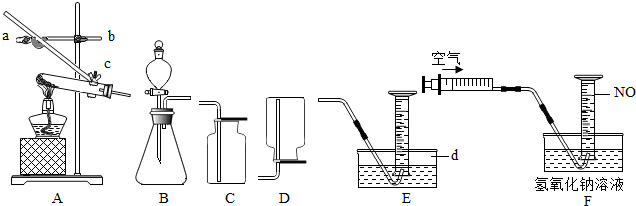
分析 据图即可知道有关仪器的名称;根据反应的化学方程式的书写方法书写反应的化学方程式;根据气体的性质确定收集气体的方法;根据测定氧气含量的方法以及氢氧化钠的腐蚀性解答,根据反应的化学方程式结合数据计算即可.
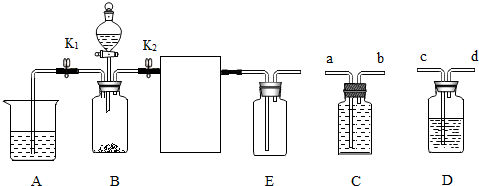
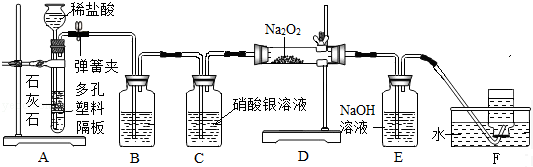
解答 解:(1据图可以看出,仪器d是水槽,故填:水槽;
(2)若要调节A中试管与酒精灯相对高度,应调节螺旋b,故填:b;
(3)氢氧化钠溶液吸收NO2反应生成亚硝酸钠、硝酸钠和水,故填:2NaOH+2NO2=NaNO2+NaNO3+H2O.
(4)实验室用稀硫酸、NaNO2饱和溶液和FeSO4•7H2O固体反应制备NO,是固液常温型反应,应选用的发生装置是B;用E装置收集纯净的NO气体,而不用C或D装置是因为一氧化氮能与氧气反应且密度与空气接近.故填:B;一氧化氮能与氧气反应且密度与空气接近;
(5)2NO+O2═2NO2
2 1 2
2NaOH+2NO2=NaNO2+NaNO3+H2O
减少的气体的体积为:60mL+20mL-67.4mL=12.6mL
氧气的体积占减少的气体体积的三分之一,故氧气的体积为:12.6mL×$\frac{1}{3}$=4.2mL;
由于氢氧化钠具有极强的腐蚀性,因此在实验中要注意氢氧化钠对皮肤的腐蚀性;
故填:4.2;氢氧化钠溶液对皮肤具有腐蚀性;
(6)60mL一氧化氮的质量为:60×10-3L×1.27g/L=0.08g
设至少需要亚硝酸钠的质量为x
2FeSO4+3H2SO4+2NaNO2═Fe2(SO4)3+2NaHSO4+2H2O+2NO↑
138 60
x 0.08g
$\frac{138}{60}=\frac{x}{0.08g}$ x=0.18g
答:至少需要固体亚硝酸钠的质量为0.18g.
点评 本题为信息给予题,完成此题,要善于从题干中提取有用的信息,然后根据学过的物质的性质进行分析推理即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可用肥皂水区别硬水和软水 | |
| B. | H2O是由一个氢分子和一个氧原子构成 | |
| C. | H2O中氧元素的化合价为-2 | |
| D. | H2O是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
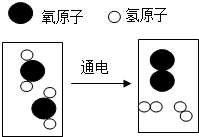 在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图:
在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 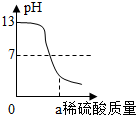 将锌片插入盛有一定量稀硫酸的烧杯中 将锌片插入盛有一定量稀硫酸的烧杯中 | |
| B. | 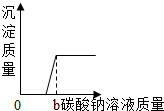 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| C. | 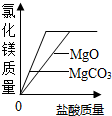 向足量碳酸镁和氧化镁固体中分别加入相同质量、相同质量分数稀盐酸中 向足量碳酸镁和氧化镁固体中分别加入相同质量、相同质量分数稀盐酸中 | |
| D. | 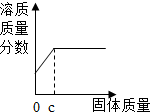 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 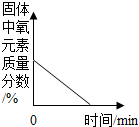 加热一定量的高锰酸钾固体 加热一定量的高锰酸钾固体 | B. | 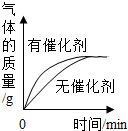 两份完全相同的过氧化氢溶液分解 两份完全相同的过氧化氢溶液分解 | ||
| C. | 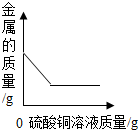 向一定量铁粉中加入硫酸铜溶液 向一定量铁粉中加入硫酸铜溶液 | D. | 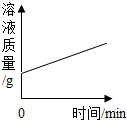 加热一定量的饱和石灰水 加热一定量的饱和石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com