
在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜。
(1)请完成该反应的化学方程式:
2Cu+2H2SO4+O2 2CuSO4+
2CuSO4+
(2)利用此反应,将含铜80%的废料与10%的稀硫酸反应转化为10%的硫酸铜溶液,计算要得到1600g10%的硫酸铜溶液,需要加入稀硫酸的质量和水的质量(假设杂质不参加反应,也不溶于水)。
(1)2H2O (2)980g 540g
解析试题分析:(1)由反应的化学方程式2Cu+2H2SO4+O2 2CuSO4+ 可知,
2CuSO4+ 可知,
反应前 反应后
Cu原子 2 2
H原子 4 0
S原子 2 2
O原子 10 8
根据质量守恒定律,化学变化前后原子的种类、数目不变,可判断另一未知生成物的分子中含有4个H原子和2个O原子,则该物质为水,短线上的化学式为2H2O。
(2)根据题给的生成的硫酸铜的质量,结合化学方程式中有关物质间的质量比,可计算出参加反应的稀硫酸中溶质的质量,以及生成水的质量,进而求出稀硫酸的质量。
解:1600g10%的硫酸铜溶液中含有硫酸铜的质量=1600g×10%=160g。
设消耗H2SO4的质量为x,生成水的质量y
2Cu + 2H2SO4 + O2= 2CuSO4 + 2H2O
196 320 36
x 160g y 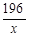 =
=
解得,x=98g =
=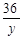
解得,y=18g
则稀硫酸溶液的质量=98g÷10%=980g
则加入水的质量=1600g-160g-18g-980g×(1-10%)=540g。
答:需要加入稀硫酸的质量为980g,加入水的质量为540g。
考点:质量守恒定律及其应用,根据化学反应方程式的计算
点评:利用质量守恒定律中的原子守恒来推断物质的化学式,是解此类题最常用的方法,学生应注意守恒思想在解题中的重要作用;根据化学方程式进行的计算,难度不大,解答时注意要有完整的计算步骤和规范的书写格式即可,此外还要明确溶液的质量=溶质的质量+溶剂的质量,这也是解答本题的关键之一。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:初中化学 来源: 题型:阅读理解
| 加热 |
| 实验过程 | 预期的实验现象 |
| 答案 | 实验过程 | 预期的实验现象 |
| 答案1 | 取适量红褐色粉末装入试管中,加热. | 试管内壁有水珠出现 |
| 答案2 | ①取适量红褐色粉末装入试管中,加入过量的稀盐酸充分反应 ②过滤,将滤纸上的黑色固体烘干后放在石棉网(或燃烧匙中)用酒精灯灼烧. (③将涂有澄清石灰水的玻璃片放在固体上方) |
试管底部有黑色固体 黑色固体保持红热,并逐渐减少 (澄清石灰水变浑浊) |
| 答案3 | 检验碳酸钙: ①取适量红褐色粉末装入试管中,加入稀盐酸. ②将生成的气体通入澄清石灰水. |
有气泡产生 澄清石灰水变浑浊 |
| 检验氢氧化镁: 取适量红褐色粉末装入试管中,加热 |
试管内壁有水珠出现 | |
| 答案4 | ①取适量红褐色粉末装入试管中,加热. ②将产生的气体通入澄清石灰水. |
试管内壁有水珠出现 澄清石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

 、
、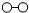 、
、 分别表示N2、H2、NH3.在催化剂表面(下图中
分别表示N2、H2、NH3.在催化剂表面(下图中 表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| △ |
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com