
【题目】中兴缺“芯”事件震惊国人。芯片是电脑、智能家庭等的核心部件,芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。
(1)硅与金刚石结构相似,则构成硅的粒子是______(填粒子名称)。
已知硅原子结构示意图为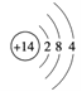 下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_____(填序号)。
下面是四种粒子的结构示意图,其中与硅的化学性质相似的是_____(填序号)。
(2)光伏发电的太阳能电池板也需用高纯硅。在日光下高纯硅的作用主要是将光能转化为______能。
(3)自然界中的硅元素主要以二氧化硅的形式存在,请写出二氧化硅的化学式______。硅胶是常用的干燥剂,其主要成分可视作二氧化硅(如图),你认为硅胶可作干燥剂的原因可能是_______(一条即可)。

(4)高纯硅的制备以石英砂(主要成分是二氧化硅)为原料,生产过程示意图如下:

①上述四个步骤中属于物理变化的是______。
②物质M是该生产过程中可循环使用的物质,写出步骤4反应的化学方程式______。
(5)因天然金刚石资源稀少,难以满足要求。人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷(CH4)等为原料制造金刚石薄膜。
下列说法不正确的是_____(写字母序号)。
A 一种元素可以组成多种性质不同的单质
B 石墨合成金刚石发生的是物理变化
C 石墨与金刚石物理性质不同是因为结构不同
D 物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
(6)不仅硅与碳具有相似化学性质,其氧化物二氧化硅和二氧化碳也有相似化学性质。试写出二氧化硅与氢氧化钠溶液反应的化学方程式_____。
(7)古代我国人民就积累了许多对物质变化的认识。春秋末期齐国的工艺官书《考工记》中载有“涑帛”的方法,即利用“灰”(草木灰)和“蜃”(贝壳灰)混合加水所得溶液来洗涤丝帛。这种溶液能洗涤丝帛主要是因为其中一定含有_____(写化学式,水除外)。(注:草木灰的主要成分为碳酸钾,贝壳灰的主要成分为氧化钙)
【答案】硅原子 ② 电 SiO2 与水反应(或具有吸水性或具有疏松多孔的结构等合理即可) 步骤3 SiHCl3+H2![]() Si+3HCl B 2NaOH+SiO2═Na2SiO3+H2O KOH
Si+3HCl B 2NaOH+SiO2═Na2SiO3+H2O KOH
【解析】
(1)金刚石是由碳原子直接构成的,硅与金刚石结构相似,构成硅的粒子是硅原子,原子的最外层电子数与物质的化学性质有密切的关系,硅原子的最外层电子数为4,所以与硅的化学性质相似的是②;故填:硅原子;②
(2)光伏发电的太阳能电池板也需用高纯硅,在日光下高纯硅的作用主要是将光能转化为电能;故填:电
(3)氧元素在化合物中通常显﹣2价,二氧化硅的化学式为:SiO2,硅胶可作干燥剂的原因可能是与水反应(或具有吸水性或具有疏松多孔的结构等合理即可);故填:与水反应(或具有吸水性或具有疏松多孔的结构等合理即可)
(4)①物理变化中没有新物质生成,上述四个步骤中属于物理变化的是步骤3;②SiHCl3和氢气在高温的条件下生成硅和氯化氢,化学方程式为SiHCl3+H2![]() Si+3HCl。故填:步骤3;SiHCl3+H2
Si+3HCl。故填:步骤3;SiHCl3+H2![]() Si+3HCl
Si+3HCl
(5)A.一种元素可以组成多种性质不同的单质,比如碳元素可以组成金刚石,石墨等单质,说法正确;故不符合题意;
B.石墨与金刚石是两种不同的单质,故石墨合成金刚石发生的是化学变化,说法错误;故符合题意;
C.石墨与金刚石物理性质不同是因为碳原子的排列方式不同,结构不同,说法正确;故不符合题意;
D.物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素还要考虑价格,环保,回收,便利等因素,说法正确;故不符合题意;
故填:B
(6)二氧化硅和二氧化碳有相似化学性质,二氧化碳与氢氧化钠反应生成碳酸钠和水,故二氧化硅与氢氧化钠反应生成硅酸钠和水,故反应方程式为2NaOH+SiO2═Na2SiO3+H2O;氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钾反应生成碳酸钙沉淀和氢氧化钾,故一定含有氢氧化钾;故填:2NaOH+SiO2═Na2SiO3+H2O;KOH


科目:初中化学 来源: 题型:
【题目】请根据下列图示装置回答问题。
(1)仪器①的名称是______。
(2)B装置可以作为很多气体的发生装置,写出能用B装置来制取气体的化学反应方程式______(写1个);
(3)若用E装置收集气体,收集满的现象是______;选用D装置收集二氧化碳气体的理由是____________。
(4)氨气是一种有刺激性气味、密度比空气小、极易溶于水的气体,实验室常用加热氯化铵和熟石灰固体混合物制取氨气。制取氨气应选择的发生装置是______(填字母),如果用图F收集氨气,气体从______(填“a”或“b”)端进入,为防止多余的氨气逸散到空气中,可用______(填写物质名称)吸收。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除 NaCl外,还含有 MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是_____。
(2)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒_____;
(3)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是我们学习化学的重要工具。下表是小华绘制的元素周期表的局部,依据此表回答问题:

(1)第14号元素的元素符号为______;
(2)地壳中含量最多的元素为_______(填元素符号),其原子的质子数是______,在化学反应中它易______(填“得到”或“失去”)电子。
(3)钠元素在元素周期表中位于第________周期。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t1℃时,将等质量的硝酸钾和氣化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氣化钾的瑢解度曲线如图2所示。则下列说法正确的是
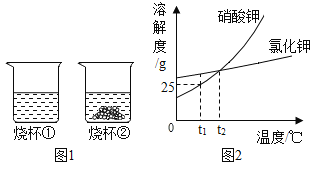
A.烧杯①的溶液一定是不饱和瑢液
B.烧杯①的溶液是硝酸钾溶液
C.烧杯②的溶液升温到t2℃时,烧杯底部还有部分物质不溶解
D.若烧杯①和烧杯②的溶液都升温到t2℃时,溶质的质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题。
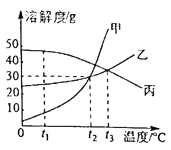
(1)随着温度的变化溶解度变化较大的种物质是__________,这类物质常采取___________的方法从溶液中获得晶体。
(2)t1℃时,甲、乙、丙三物质的溶解度由大到小的顺序是__________________
(3)t2℃时,甲和乙的溶解度__________(填“相等”或“不相等”)。
(4)t2℃时,甲物质的饱和溶液中溶质与溶剂的质量比为__________(写最简比)。
(5)t3℃时,将乙和丙两种物质的饱和溶液降低到t1℃,所得溶液中溶质的质量分数大小关系为:乙____丙(填“>”或“<”或“=”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,化学与生活息息相关.通过一学期的学习,请你回答下列问题.
(1)在日常生活中饮用水硬度过大的水不利于人体健康,日常生活中常用___来区分硬水和软水,可用___的方法降低水的硬度,实验室中常用___的方法除去不溶于水的杂质.
(2)防毒面具中使用了活性炭,这时利用了活性炭的___作用.
(3)天然气的主要成分为___(填化学式),其燃烧的化学方程式是___.
(4)煤燃烧生成CO2、SO2、CO等气体,其中会引起温室效应的是__;溶于水会形成酸雨的是__;能与人体血红蛋白结合的是___.
(5)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4═Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为___.
(6)查阅资料可知,米酒味道变酸是因为米酒中产生的醋酸杆菌使乙醇(C2H5OH)和氧气发生反应生成了醋酸(CH3COOH)和另一种常见的液体.食物变质是一种___氧化反应(填“剧烈”、“缓慢”).米酒味道变酸的化学反应方程式为___;可用___验证米酒味道变酸是生成了醋酸.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有60g 15%的氢氧化钡溶液的烧杯中,缓慢滴加稀硫酸至过量。烧杯中的某些量随着稀硫酸的滴加,其变化趋势肯定错误的是( )
A. 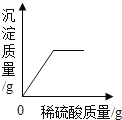 B.
B. 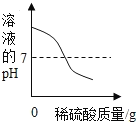
C. 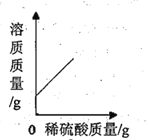 D.
D. 
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方案,不能达到相应实验目的的是( )
A.  比较空气与人体呼出的气体中 CO2 含量
比较空气与人体呼出的气体中 CO2 含量
B.  探究 MnO2 能否加快 H2O2 分解
探究 MnO2 能否加快 H2O2 分解
C.  验证燃烧需要温度达到着火点
验证燃烧需要温度达到着火点
D.  探究 CO2 对铜生锈是否有影响
探究 CO2 对铜生锈是否有影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com