
| A. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| B. | 在空气中打开盛浓盐酸的试剂瓶瓶塞,产生白雾 | |
| C. | 在电解水实验中,与电源正负极相连的两极上产生的气体体积比约为2:1 | |
| D. | 取少量氢氧化钠固体露置在空气中,其表面潮湿并逐渐溶解 |
分析 A、根据硫在氧气中燃烧的现象进行分析判断.
B、根据浓盐酸的物理性质进行分析判断.
C、根据电解水实验的现象进行分析判断.
D、根据氢氧化钠的性质进行分析判断.
解答 解:A、硫在氧气中燃烧,发出明亮的蓝紫色火焰,放出热量,产生一种具有刺激性气味的气体,故选项说法正确.
B、浓盐酸具有挥发性,挥发出的氯化氢气体与空气中的水蒸气凝结成盐酸小液滴悬浮在空气中形成白雾.故选项说法正确.
C、在电解水实验中,与电源正负极相连的两极上产生的气体体积比约为1:2,故选项说法错误.
D、取少量氢氧化钠固体露置在空气中,其表面潮湿并逐渐溶解;故选项说法正确.
故选C.
点评 本题难度不大,掌握常见物质燃烧的现象、酸的物理性质、碱的化学性质等即可正确解答.


科目:初中化学 来源: 题型:选择题
| A. | 蜡烛刚刚熄灭时产生的白烟是二氧化碳气体 | |
| B. | 氢氧化钠固体易潮解,可做某些气体的干燥剂 | |
| C. | 二氧化碳不供给呼吸,不宜作为植物的养料 | |
| D. | 大量使用化石燃料会造成大气污染,应该停止对化石燃料的开采和利用 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
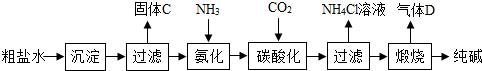
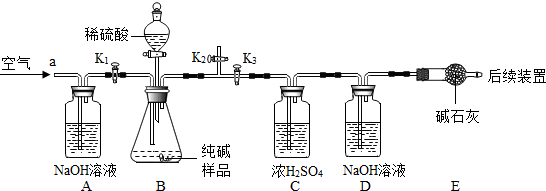
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则四种说法正确的个数为( )
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则四种说法正确的个数为( )| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 在实验中经常出现实验现象与理论的“不配合”,理性思考这些现象有助于提高我们的科学素养.
在实验中经常出现实验现象与理论的“不配合”,理性思考这些现象有助于提高我们的科学素养.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙醇属于可再生能源 | |
| B. | “可燃冰”将成为未来的新能源 | |
| C. | 将煤碳加工成蜂窝煤,能使煤燃烧更充分 | |
| D. | 化学电池是将化学能传化为热能的一种方式 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸). | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为: CaCl2+Na2CO3═CaCO3↓+2NaCl(或Na2CO3+2HCl═2NaCl+H2O+CO2↑). |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
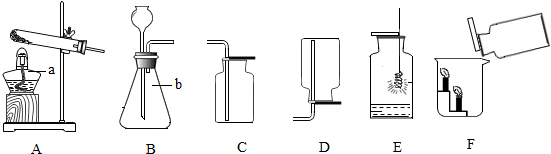
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com