
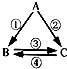
 已知A、B、C是初中化学的常见物质,其相互关系如图所示.若A、B是组成元素相同且常温下都为液态的氧化物,C为供给呼吸,则A的化学式为H2O2,C为化学式为O2,反应①的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
已知A、B、C是初中化学的常见物质,其相互关系如图所示.若A、B是组成元素相同且常温下都为液态的氧化物,C为供给呼吸,则A的化学式为H2O2,C为化学式为O2,反应①的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. 分析 过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气能够供给呼吸;
电解水生成氢气和氧气,氢气燃烧生成水.
解答 解:过氧化氢和水都是由氢元素和氧元素组成的物质,并且都是氧化物,过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气能够供给呼吸;
电解水生成氢气和氧气,氢气燃烧生成水,因此ABC分别是过氧化氢、水和氧气;
则A的化学式为H2O2,C为化学式为O2,过氧化氢分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:H2O2;O2;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题主要考查物质的性质,只要掌握了各种物质的性质,解答起来就比较简单了.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
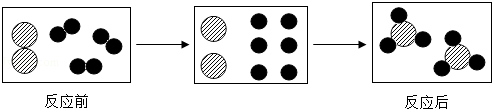
| A. | 反应前后分子种类不发生改变 | |
| B. | 反应前后原子的种类和数目发生改变 | |
| C. | 反应前两种分子的个数比是1:2 | |
| D. | 该反应遵守质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
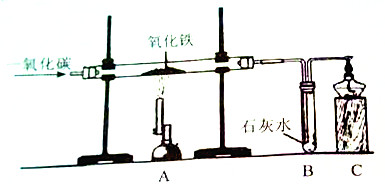
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
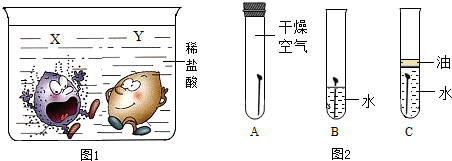
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com