
分析 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.由题意“2.4g某物质在氧气中完全燃烧,生成2.2g二氧化碳、1.8g水和3.2g二氧化硫”,则可计算1.8g水中氢元素的质量,即2.4g该物质含氢元素的质量.
解答 解:1.8g水中氢元素的质量=1.8g×$\frac{2}{18}$=0.2g,根据质量守恒定律可知,水中氢元素的质量即该物质中氢元素的质量.根据质量守恒定律,则参加反应的氧气的质量为2.2g+1.8g+3.2g-2.4g=4.8g,因此该反应方程式中氧气和二氧化硫的化学计量数之比为$\frac{4.8g}{32}$:$\frac{3.2g}{64}$=3:1.
故答案为:0.2g;3:1.
点评 本题是运用化学中的基本思想质量守恒思想,学会处理此类计算的题目,从而培养了学生的创新思维能力.


科目:初中化学 来源: 题型:实验探究题
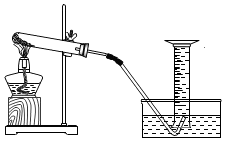 在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.
在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验,老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克.②实验设计4组.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
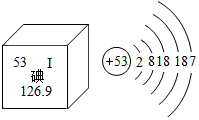 美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖.如图下列关于碘的说法错误的是( )
美国两位科学家通过对碘元素的研究,揭示了“细胞如何感知周围环境”之谜,从而获得诺贝尔化学奖.如图下列关于碘的说法错误的是( )| A. | 碘的相对原子质量约为126.9g | |
| B. | 碘元素与钙元素形成化合物的化学式为CaI2 | |
| C. | 碘元素与氯元素具有相似的化学性质 | |
| D. | 碘原子的核电荷数=质子数=核外电子数=53 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
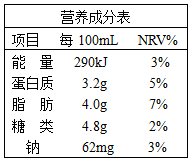 我国《预包装食品营养标签通则》规定,预包装食品标签上必须标示出能量、蛋白质、脂肪、糖类和钠的含量值. 如图为某奶制品各项含量.
我国《预包装食品营养标签通则》规定,预包装食品标签上必须标示出能量、蛋白质、脂肪、糖类和钠的含量值. 如图为某奶制品各项含量.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③②④⑥⑤ | B. | ③①②④⑥⑤ | C. | ①③②④⑤⑥ | D. | ③①②④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
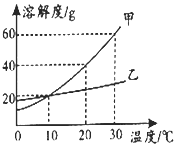
| A. | 20℃时甲和乙的饱和溶液,升温到30℃时仍为饱和溶液 | |
| B. | 甲和乙的溶解度相等 | |
| C. | 10℃时,甲和乙各10 g分别加入到50g水中,均形成饱和溶液 | |
| D. | 10℃时,将甲和乙两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com