


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2012-2013学年福建省厦门市业质量检查化学试卷(解析版) 题型:填空题
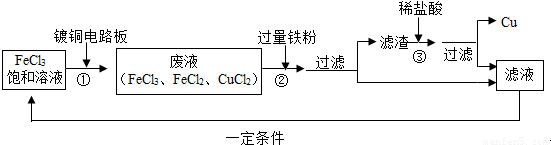
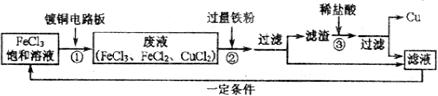
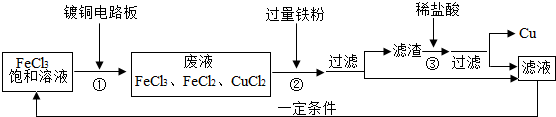
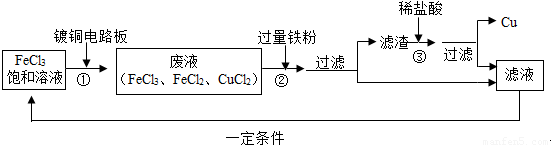
氯化铁溶液能腐蚀铜,工业上常用此原理生产印刷线路板.以下是印刷线路板的生产及废液的处理过程:
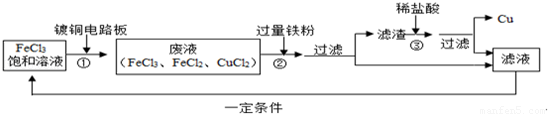
请回答下列问题:
(1)步骤②中发生了两个反应:2FeCl3+Fe═3FeCl2和 .
(2)滤渣的成份有 和 ,步骤③中发生反应的化学方程式是 .
查看答案和解析>>
科目:初中化学 来源:2009年江苏省“化学与可持续发展”化学活动周初中化学竞赛初赛试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com