
【题目】中和反应是一类重要的化学反应。某同学利用图1实验研究稀盐酸与氢氧化钠液反应的过程,并测量反应过程中溶液的pH和温度的变化情况,得到图2和图3
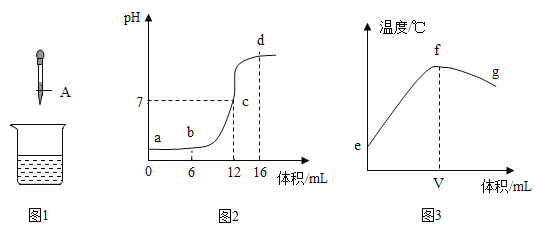
(1)烧杯中发生反应的化学方程式为_____;
(2)滴管A中溶液的溶质是_____(填化学式);
(3)结合图2中有关信息可知图3中V的数值最接近_____(填“6”、“12”或“16”);
(4)下列说法正确的是_____。
A 图2中b点所示溶液中的溶质是NaCl和HCl
B 取图2中d点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加
D 图3中e→f变化趋势可说明该反应是放热反应
【答案】![]() NaOH 12 AD
NaOH 12 AD
【解析】
(1)烧杯中发生反应为稀盐酸与氢氧化钠生成氯化钠和水,化学方程式为NaOH + HCl =NaCl + H2O;
(2)由图2可知,溶液的pH逐渐增大,可知是将氢氧化钠溶液滴入盐酸中,滴管A中溶液的溶质是氢氧化钠;
(3)中和反应放热,图3中V对应的温度最高,说明氢氧化钠和盐酸刚好完全反应,溶液的pH为7,结合图2可知,数值最接近12;
(4)A、图2中b点所示溶液中pH<7溶液呈酸性,盐酸有剩余,溶液中的溶质是NaCl和HCl,选项正确;
B、图2中d点氢氧化钠过量,所示溶液溶质是氯化钠和氢氧化钠,加热蒸干所得固体为氯化钠、氢氧化钠,为混合物,选项错误;
C、在c点盐酸和氢氧化钠恰好完全反应,c→d所示溶液中,氯化钠的质量不会增加,选项错误;
D、图3中e→f溶液温度不断升高,变化趋势可说明该反应是放热反应,选项正确。
故选AD。


科目:初中化学 来源: 题型:
【题目】某同学进行下图两个实验。
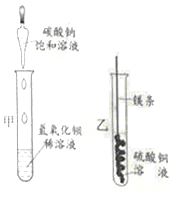
(l)甲实验中反应的化学方程式为____________;
(2)乙实验观察到的现象是___________,溶液由蓝色变成无色。
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
【查阅资料】硫酸钡不溶于酸。
【提出猜想】 白色沉淀为:Ⅰ._______;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为____________。 ②若______且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,________,猜想Ⅲ成立。 |
【拓展与思考】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时___________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
(1)金属活动性顺序表: K Ca Na___________Sn Pb(H) Cu Hg Ag Pt Au
(2)同学们选了三组物质来比较锌、铁、铜三种金属的活动性:
①Zn、Fe、 Cu、稀硫酸
②Fe、ZnSO4溶液、CuSO4 溶液
③ZnSO4溶液、FeSO4 溶液、Cu
仅用组内物质就能达到目的的是____________ (填序号)。
(3)用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如下图所示。试回答:
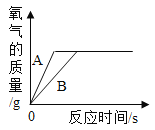
①曲线A表示的是____________(填“铁”或“锌”)跟稀硫酸反应的情况。
②上述曲线图除能说明①的结论外,还可得出的结论是(答一条)__________________。
(4)小明从实验废液中回收铜,得到的铜样品中含有少量铁粉,为测定样品中铜的质量分数,利用以下方案进行实验: ![]() ,将固体洗涤、干燥、称量为10.8g,请写出发生反应的化学方程式_____________________________,测得样品中铜的质量分数为__________________。
,将固体洗涤、干燥、称量为10.8g,请写出发生反应的化学方程式_____________________________,测得样品中铜的质量分数为__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】温度不变,对100 mL氯化钠饱和溶液进行如图所示实验。下列结论不正确的是
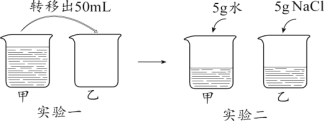
A. 实验一后,甲和乙中溶质质量分数相等B. 实验二后,乙溶液溶质质量分数增大
C. 实验二后,甲溶液变为不饱和溶液D. 实验二后,甲和乙溶液中溶质质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有如图甲所示仪器和装置,请回答下列问题:
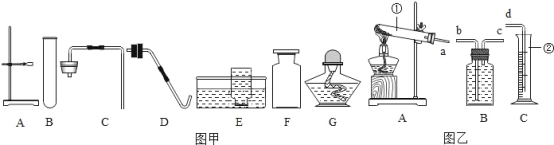
(1)写出A、G两种仪器的名称:A:_____;G:_____。
(2)用加热氯酸钾和二氧化锰的方法制取一瓶较为纯净的氧气,应从图甲中选用的仪器装置是_________(填字母编号),该实验的主要步骤有:①装药品;②检查装置的气密性;③加热;④将装置固定在铁架台上;⑤熄灭酒精灯;⑥收集气体;⑦将导管移出水槽。正确的操作顺序为_____,反应的文字表达式为_____,其中二氧化锰起_____作用。
(3)某校化学兴趣小组的同学利用如图乙所示装置进行实验。
(实验目的)粗略测定加热2g高锰酸钾所收集到的氧气体积。
(反应原理)高锰酸钾制取氧气的文字表达式为_____。
(装置连接)为达到实验目的,各装置的正确连接顺序是:a→_____→d。
(补充实验)在收集到的氧气中做细铁丝燃烧的实验:
①集气瓶内为什么要预先装少量水或铺一层细砂_____。
②实验过程中发现B瓶中的水变红了,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示某些物质间的转化关系(反应条件均略去),其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属。B、D、E均为无色气体。请回答:

(1)X可以是___________。
(2)B物质固体时的名称是___________。
(3)上述转化过程中没有涉及到的四大基本反应类型是___________。
(4)写出G与E反应的化学方程式________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】啤酒盖(主要成分为铁)生锈直接影响啤酒厂家的市场销售和品牌形象。某小组同学用铁钉代替啤酒盖模拟其生锈实验,探究铁生锈的条件及影响生锈速率的因素。
I.探究铁生锈的条件
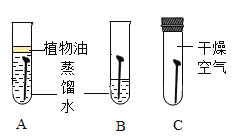

(1)证明铁生锈需要与氧气接触的实验现象是____。
II.探究影响铁生锈速率的因素
(查阅资料)啤酒的pH值大约在3.8~4.6之间
(猜想假设)铁钉生锈可能与溶液酸碱度、温度、是否杀菌有关。
实验1:分别取铁钉浸于等体积液体中,在空气中放置相同时间进行如下实验:
实验 | 是否杀菌 | pH值 | 温度/℃ | 锈蚀情况/% |
① | 杀菌 | 6 | 20 | 无现象 |
② | 杀菌 | 6 | 70 | 较明显生锈 |
③ | 未杀菌 | 6 | 70 | 明显生锈 |
④ | 未杀菌 | 6 | 20 | 略微生锈 |

实验2:在70℃时,将杀菌后的铁钉于等体积溶液中,在空气中放置相同时间进行如下实验:
实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
pH值 | 3 | 5 | 7 | 9 | 11 |
锈蚀情况 | 完全生锈 | 明显生锈 | 略微生锈 | 无现象 | 无现象 |
(解释与结论):
(2)由实验1得出“温度与铁生锈速率有关”的结论,依据的两个实验是__(填编号)
(3)实验2的目的是_______。
(4)由实验1和实验2推知影响铁生锈的因素是_____
(反思与评价)
(5)实验2没有进行pH=13的实验,理由是 ___。
(6)结合本题请分析啤酒盖易生锈的原因是 ______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从2019年春节起,常州大部分地区禁止燃放烟花爆竹,开启了龙城环保新时代。
(1)禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还可以减少SO2和_________等空气污染物的排放,提升空气质量。
(2)秸杆在一定条件下发酵,可以逐步转化为乙醇,乙醇发生不完全燃烧,其微观过程可表示为(“![]() ”表示碳原子、“
”表示碳原子、“![]() ”表示氢原子,“
”表示氢原子,“![]() ”表示氧原子)
”表示氧原子)
![]()
从其微观过程可以推出,乙醇的化学式为_________,a与b的比值为________。
(3)当9.2g乙醇参加上述反应过程时,产生一氧化碳的质量是多少克_____?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com