
·ÖĪö øł¾ŻŅŃÓŠµÄĪļÖŹµÄ¹¹³É”¢Ō×ӵĹ¹³ÉŅŌ¼°·Ö×ÓŗĶŌ×ÓÖ®¼äµÄ¹ŲĻµ½ųŠŠ·ÖĪö½ā“š¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©Ļą¶ŌŌ×ÓÖŹĮæŌ¼ĪŖÖŹ×ÓŹżÓėÖŠ×ÓŹżÖ®ŗĶ£¬¹ŹĢī£ŗ¢Ł£»¢Ś£»
£Ø2£©ŌŖĖŲµÄÖÖĄąÖ÷ŅŖČ”¾öÓŚŌ×ÓµÄÖŹ×ÓŹż£¬¹ŹĢī£ŗ¢Ł£»
£Ø3£©Ō×ÓÖŠŅ»¶ØĻąµČµÄŹĒÖŹ×ÓŹżÓėµē×ÓŹż£¬¹ŹĢī£ŗ¢Ł£»¢Ū£»
£Ø4£©»Æѧ±ä»ÆµÄŹµÖŹŹĒ·Ö×Ó·Ö³ÉŌ×Ó£¬Ō×ÓÖŲŠĀ×éŗĻ³ÉŠĀµÄ·Ö×Ó£¬ĖłŅŌ»Æѧ±ä»ÆÖŠŌ×Ó²»±ä”¢·Ö×ÓŅ»¶Ø±ä£¬¹ŹĢī£ŗ¢Ž£»¢Ü£®
µćĘĄ ÕĘĪÕĪļÖŹµÄ¹¹³ÉŗĶŌ×Ó¹¹³ÉŅŌ¼°Ī¢Į£µÄ×÷ÓĆŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£®


 ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø
ѧŅµ²āĘĄŅ»æĪŅ»²āĻµĮŠ“š°ø Š”ѧæĪŹ±×÷ŅµČ«ĶØĮ·°øĻµĮŠ“š°ø
Š”ѧæĪŹ±×÷ŅµČ«ĶØĮ·°øĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
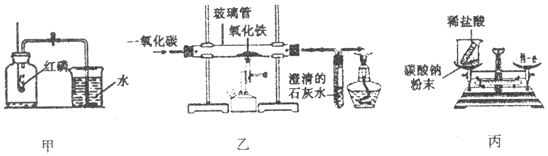
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
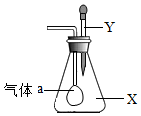 ČēĶ¼ĖłŹ¾£¬×¶ŠĪĘæÄŚŹ¢ÓŠĘųĢåX£¬µĪ¹ÜÄŚŹ¢ÓŠŅŗĢåY£¬Čō¼·Ń¹µĪ¹Ü½ŗĶ·£¬Ź¹ŅŗĢåYµĪČėĘæÖŠ£¬Õńµ“£¬Ņ»»į¶łæɼūŠ”ĘųĒņa¹ÄĘš£®ĘųĢåXŗĶŅŗĢåYæÉÄÜŹĒ£Ø””””£©
ČēĶ¼ĖłŹ¾£¬×¶ŠĪĘæÄŚŹ¢ÓŠĘųĢåX£¬µĪ¹ÜÄŚŹ¢ÓŠŅŗĢåY£¬Čō¼·Ń¹µĪ¹Ü½ŗĶ·£¬Ź¹ŅŗĢåYµĪČėĘæÖŠ£¬Õńµ“£¬Ņ»»į¶łæɼūŠ”ĘųĒņa¹ÄĘš£®ĘųĢåXŗĶŅŗĢåYæÉÄÜŹĒ£Ø””””£©| A£® | XŹĒCO2£¬YŹĒĒāŃõ»ÆÄĘ | B£® | XŹĒO2£¬YŹĒĻ”H2SO4£ØĻ”ĮņĖį£© | ||
| C£® | XŹĒN2£¬YŹĒĻ”ŃĪĖį | D£® | XŹĒCO£¬YŹĒĒāŃõ»ÆÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
| ĪĀ¶Č£Ø”ę£© | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| Čܽā¶Č£Øg£© | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 168 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
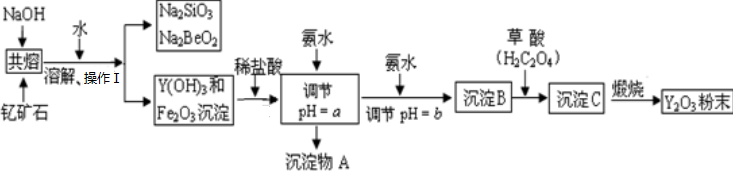
| æŖŹ¼³ĮµķŹ±µÄpH | ĶźČ«³ĮµķŹ±µÄpH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
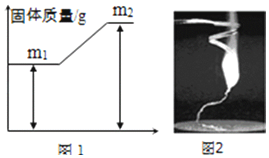
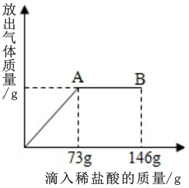 ŌŚŅ»ÉÕ±ÖŠŹ¢ÓŠÓÉNa2CO3ŗĶNaCl””×é³ÉµÄ¹ĢĢå»ģŗĻĪļ25g£¬ĻņĘäÖŠÖš½„µĪ¼ÓČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĻ”ŃĪĖį£¬·Å³öĘųĢåµÄÖŹĮæÓėµĪČėĻ”ŃĪĖįµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£ØŅŃÖŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2CO3+2HCl=2NaCl+CO2”ü+H2O£©£®Ēė·ÖĪöĒśĻßĶ¼ŗó»Ų“šĻĀĮŠĪŹĢā£ŗ
ŌŚŅ»ÉÕ±ÖŠŹ¢ÓŠÓÉNa2CO3ŗĶNaCl””×é³ÉµÄ¹ĢĢå»ģŗĻĪļ25g£¬ĻņĘäÖŠÖš½„µĪ¼ÓČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĻ”ŃĪĖį£¬·Å³öĘųĢåµÄÖŹĮæÓėµĪČėĻ”ŃĪĖįµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£ØŅŃÖŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2CO3+2HCl=2NaCl+CO2”ü+H2O£©£®Ēė·ÖĪöĒśĻßĶ¼ŗó»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com