

分析 (1)常见的净化水的方法按照净化程度由低到高的顺序是沉降、过滤、吸附、蒸馏等流程;根据吸附过程解答;
(2)根据物质化学式的写法解答;
(3)根据化合物中正负化合价的代数和为零解答;
(4)铝和稀硫酸反应生成硫酸铝和氢气解答;
(5)根据硬水中含有较多的钙、镁离子,加热煮沸可以将硬水软化成软水.
解答 解:(1)在自来水厂为了将小颗粒泥尘沉降下来,常用絮凝剂,经常使用的絮凝剂是明矾,为了除去不溶于水的固体杂质,必须用过滤的方法;在过滤后的水中仍然含有可溶性的有色、有异味的物质,通常用吸附剂来吸附,吸附能力较强的是活性炭;
(2)氢氧化铝的化学式为:Al(OH)3;一般含有碳元素的化合物是有机物,三氯甲烷(CHCl3)属于有机物;
(3)化合物中正负化合价的代数和为零,设铁元素的化合价是x
(+1)×2+x+(-2)×4=0
x=+6
(4)铝和稀硫酸反应生成硫酸铝和氢气,反应的化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑;
(5)自来水厂的净水过程不能将硬水软化成软水,生活中将硬水软化的方法是煮沸.
答案:
(1)过滤;活性炭;
(2)Al(OH)3;有机物;
(3)+6;
(4)2Al+3H2SO4=Al2(SO4)3+3H2↑;
(5)不能;煮沸.
点评 本题难度不大,掌握水的净化方法、过滤操作、硬水和软水的检验以及物理变化和化学变化的判别方法即可正确解答本题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除去杂质的方法 | |
| A | NaCl | 泥沙 | 溶解、过滤、蒸发 |
| B | N2 | O2 | 通过灼热的铜网 |
| C | NaOH溶液 | Na2CO3 | 加入稀盐酸至不再产生气泡 |
| D | CO | CO2 | 先通过足量的氢氧化钠溶液,再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
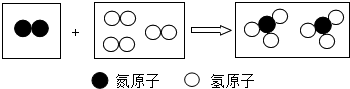 如图是某反应的微观过程.
如图是某反应的微观过程.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 固体A | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 固体B | 13.3 | 31.6 | 63.9 | 110 | 169 | |
| 固体C | 35.0 | 44.5 | 57.6 | 55.0 | 50.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 非金属元素 | Si | P | S | Cl | |
| 最高价含氧酸 | 名称 | (偏)硅酸 | 磷酸 | 硫酸 | 高氯酸 |
| 化学式 | H2SiO3 | H3PO4 | H2SO4 | HClO4 | |
| 酸性 | 弱 | 中强 | 强 | 强 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③⑤⑥ | B. | ①②④⑥ | C. | ①②④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | pH:酸雨>正常雨水 | |
| B. | 常温条件下在水中的溶解性:氢氧化钙>氢氧化钠 | |
| C. | 溶于水后溶液的温度:氢氧化钠>硝酸铵 | |
| D. | 所有原子中:质子数>核外电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冬天用煤炉取暖,为防止热量散失,应关紧门窗 | |
| B. | 进入干涸的深井前,应先做灯火试验 | |
| C. | 用NaHCO3治疗胃酸过多 | |
| D. | 铵态氮肥与熟石灰混合使用会降低肥效 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com