
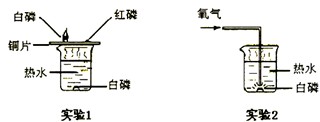
科目:初中化学 来源: 题型:阅读理解
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一 | 取少量滤液于试管中,在滤液中插入一根铜丝 | 铜丝表面无变化 铜丝表面无变化 |
猜想①成立 |
铜丝表面有银白色固体析出 铜丝表面有银白色固体析出 |
猜想②成立 | ||
| 方案二 | 取少量滤液于试管中,滴加几滴稀盐酸 取少量滤液于试管中,滴加几滴稀盐酸 |
滤液无明显变化 滤液无明显变化 |
猜想①成立 |
生成白色沉淀 生成白色沉淀 |
猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
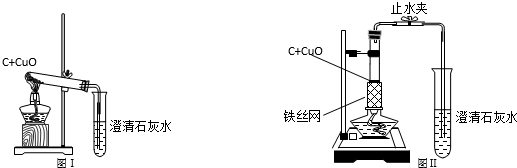
| 比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
| 时间 | 1'51〃 | 1'43〃 | 1'57〃 | 1'51〃 | 1'51〃 | 1'53〃 | 4' |
| 实验现象 | 红热,产生大量气泡,澄清石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
| 实验结果 | 表层铜珠较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成Cu2O | 主要产物是Cu2O | |||
查看答案和解析>>
科目:初中化学 来源:山东省中考真题 题型:实验题
小娜及学习小组的同学在老师的指导下对黄铜中铜和锌的含量及其性质展开了探究。
【查阅资料】
HCl+AgNO3=AgCl ↓+HNO3,AgCl 是一种白色沉淀,这个反应在化学上用于检验和鉴别。
【提出问题】测定黄铜中锌、铜的质量分数。
【实验原理及实验方案设计】(略)。
Ⅰ【探究实验】
1. 先将黄铜在热碱液中浸泡一段时间,以除去表面的油污。然后再放在稀盐酸中浸泡片刻,其目的是_________________________ 。用蒸馏水清洗干净,干燥,取少量研碎,称取质量为ag 。
2. 将ag 试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应。
3. 将小烧杯中的混合物过滤,_____________( 请将此实验步骤补充完整) 。
4. 称取固体的质量为bg 。
5. 计算出黄铜中锌和铜的质量分数。
Ⅱ【反思与评价】 在步骤1 中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将 (填“偏大”、“偏小”或“不受影响”)
Ⅲ【拓展探究】
1. 重复【探究实验】步骤1 。
2. 将ag 试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
(1 )锌和硝酸盐溶液反应的化学方程式是________________________ 。
(2 )同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为______________ 。
(3 )设计两种实验方案来验证以上猜想。

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
小娜及学习小组的同学在老师的指导下对黄铜中铜和锌的含量及其性质展开了探究。
【查阅资料】
HCl+AgNO3=AgCl↓+HNO3,AgCl是一种白色沉淀,这个反应在化学上用于检验和鉴别。
【提出问题】测定黄铜中锌、铜的质量分数。
【实验原理及实验方案设计】(略)。
【探究实验】
1.先将黄铜在热碱液中浸泡一段时间,以除去表面的油污。然后再放在稀盐酸中浸泡片刻,其目的是_________________________。用蒸馏水清洗干净,干燥,取少量研碎,称取质量为ag。
2.将ag试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应。
3.将小烧杯中的混合物过滤,_____________(请将此实验步骤补充完整)。
4.称取固体的质量为bg。
5.计算出黄铜中锌和铜的质量分数。
【反思与评价】
在步骤1中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将(填“偏大”、“偏小”或“不受影响”)
【拓展探究】
1.重复【探究实验】步骤1。
2.将ag试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
(1)锌和硝酸盐溶液反应的化学方程式是________________________。
(2)同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为______________。
(3)设计两种实验方案来验证以上猜想。
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一 | 取少量滤液于试管中,在滤液中插入一根铜丝 | ________________ | 猜想①成立 |
| ________________ | 猜想②成立 | ||
| 方案二 | _________________________ _________________________ | ________________ | 猜想①成立 |
| ________________ | 猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
小娜及学习小组的同学在老师的指导下对黄铜中铜和锌的含量及其性质展开了探究。
【查阅资料】
HCl+AgNO3=AgCl↓+HNO3,AgCl是一种白色沉淀,这个反应在化学上用于检验和鉴别。
【提出问题】测定黄铜中锌、铜的质量分数。
【实验原理及实验方案设计】(略)。
【探究实验】
1.先将黄铜在热碱液中浸泡一段时间,以除去表面的油污。然后再放在稀盐酸中浸泡片刻,其目的是_________________________。用蒸馏水清洗干净,干燥,取少量研碎,称取质量为ag。
2.将ag试样放入小烧杯中,加入足量稀盐酸,搅拌使其充分反应。
3.将小烧杯中的混合物过滤,_____________(请将此实验步骤补充完整)。
4.称取固体的质量为bg。
5.计算出黄铜中锌和铜的质量分数。
【反思与评价】
在步骤1中,若试样用蒸馏水洗涤之后,不干燥,则计算出合金中锌的质量分数将 (填“偏大”、“偏小”或“不受影响”)
【拓展探究】
1.重复【探究实验】步骤1。
2.将ag试样放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
(1)锌和硝酸盐溶液反应的化学方程式是________________________。
(2)同学们对蓝色滤液中所含的溶质做出多种猜想,其中只有两种猜想可能成立,这两种猜想是:①溶质为硝酸锌和硝酸铜;②溶质为______________。
(3)设计两种实验方案来验证以上猜想。
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一] | 取少量滤液于试管中,在滤液中插入一根铜丝 | ________________ | 猜想①成立 |
| ________________ | 猜想②成立 | ||
| 方案二 | _________________________ _________________________ | ________________ | 猜想①成立 |
| ________________ | 猜想②成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com