


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
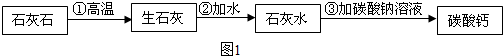
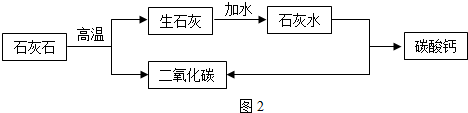
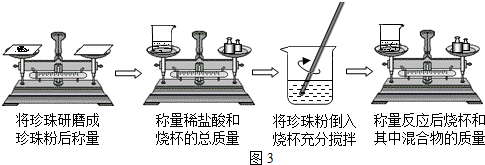
| 编号 | 反应前 | 反应后 | |
| 烧杯和稀盐酸的质量 | 珍珠粉的质量 | 烧杯和其中混合物的质量 | |
| 甲 | 150.0g | 2.8g | 151.7g |
| 乙 | 150.0g | 0.28g | 150.17g |
查看答案和解析>>
科目:初中化学 来源: 题型:
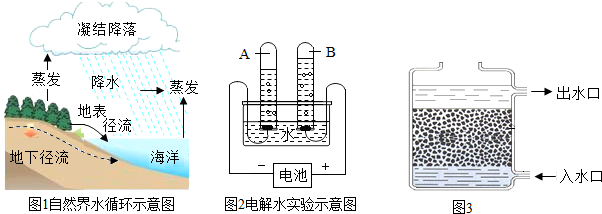
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
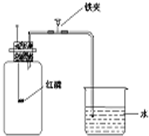 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com