
向装有等量水的A、B、C烧杯中分别加入10 g、
25 g、25 g NaNO3固体,充分溶解后,现象如图一所示。
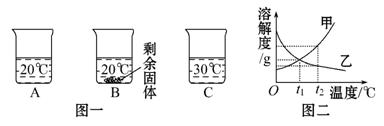
(1)烧杯中的溶液一定属于饱和溶液的是 (填序号);
(2)图二中能表示NaNO3溶解度曲线的是 (填“甲”或“乙”);
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是 ________;
(4)由图二分析,若分别将100 g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是 (填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
(1)A、C中固体完全溶解不能判断是否是饱和溶液,B中固体有剩余,一定是饱和溶液。(2)由图一可以看出,NaNO3的溶解度随着温度的升高而增大,所以甲应该是NaNO3的溶解度曲线。(3)要使剩余的固体溶解,可以加水或升高温度。(4)由于乙的溶解度随着温度的降低而增大,所以从t2℃降到t1℃乙变成不饱和溶液,A叙述不正确;t2℃甲的溶解度比乙大,100 g饱和溶液中所含的溶质甲比乙多,则溶剂的量甲小于乙,从t2℃降到t1℃,溶液中溶剂的质量不变,B叙述是正确的;从t2℃降到t1℃,甲析出晶体,乙溶液质量不变,所以溶液的质量甲应小于乙,C叙述不正确;t2℃时甲的溶解度大于乙的溶解度。故该温度下甲饱和溶液溶质的质量分数大于乙饱和溶液溶质的质量分数,降温至t1℃时甲溶解度降低,析出晶体,为t1℃时饱和溶液,乙的溶解度增大,溶质质量分数不变。由于甲t1℃时的溶解度大于t2℃时乙的溶解度,故t1℃时甲的溶质质量分数大于乙的溶质质量分数。
答案:(1)B (2)甲 (3)加水(或升温) (4)B、D


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
青铜是人类最早使用的铜锡合金,下列说法中不正确的是
( )
A.青铜属于纯净物 B.青铜属于金属材料
C.青铜的硬度比铜大 D.青铜耐腐蚀,易铸造成形
查看答案和解析>>
科目:初中化学 来源: 题型:
小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习。
【查阅资料】真金在空气中不会生锈,生满铜绿的“金戒指”材质为铜锌合金;铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜,碱式碳酸铜受热易分解生成CuO、H2O和CO2。据上述资料可推知,碱式碳酸铜由__________种元素组成。
【实验探究】将该枚戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色。
⑴小明认为:气体 中除了含有CO2,还可能含有少量__________。实验室常用__________的方法检验这种可能含有的气体。
中除了含有CO2,还可能含有少量__________。实验室常用__________的方法检验这种可能含有的气体。
⑵小红认为蓝绿色溶液中的溶质只有氯化锌。小华认为溶液中的溶质除了氯化锌外,还应该含有____________________。他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了观察:①______________________________,②______________________________,证实了自己的观点。
⑶小娟取适量新制的FeCl2溶液,加入锌粒,一段时间后,溶液颜色变浅。结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
配制溶质质量分数为5%的下列溶液,能达到目的的是 ( )
A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌
B.称取5.0 g氯化钾,放入100 mL水中,充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
查看答案和解析>>
科目:初中化学 来源: 题型:
已知金属钠和水能发生下列反应:
2Na+2H2O====2NaOH+H2↑,现将一定质量的金属钠放入75.6克水中,反应后生成8克氢氧化 钠,计算:
钠,计算:
(1)参加反应的水是多少克?
(2)反应后得到的氢氧化钠溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
固体CO2又称干冰,易升华。干冰灭火器常用于扑救档案资料室发生的火灾。下列关于干冰灭火的说法不正确的是( )
A.干冰升华时吸热,降低可燃物的着火点
B.CO2覆盖在可燃物表面,隔绝空气
C.CO2不能支持燃烧
D.干冰升华后不污染档案资料
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学需测定某100g过氧化氢溶液中所含过氧化氢的质量.他取10g二氧化锰放入烧杯中,并将该过氧化氢溶液全部加入,不同时间用电子天平测量其质量,所得读数如表所示:
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质总质量/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
(1)试分析,100g过氧化氢溶液完全反应后生成氧气的质量为 .
(2)计算100g过氧化氢溶液中过氧化氢质量分数为多少?(写出计算过程)
(3)请分析该方法测定结果可能会偏大的原因有 (写出一点即可).
查看答案和解析>>
科目:初中化学 来源: 题型:
把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示,下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前的质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后的质量/g | 待测 | 19.4 | 0 | 3.6 |
A.物质C一定是化合物,物质D可能是单质
B.反应后密闭容器中A的质量为19.7 g
C.反应中,物质B和物质D质量比为87:36
D.该反应为化合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com