
”¾ĢāÄæ”æAE ĪŖ³õÖŠ»ÆѧĪåÖÖ²»Ķ¬Ąą±šµÄ³£¼ūĪļÖŹ”£ŅŃÖŖ C ŗ¬ÓŠČżÖÖŌŖĖŲ£¬E ĪŖŹĄ½ēÄź²śĮæ×īøߵĽšŹō£¬A ŹĒĻą¶Ō·Ö×ÓÖŹĮæĪŖ 160 µÄĄ¶É«ČÜŅŗ”£ĖüĆĒÖ®¼äĻą»„¹ŲĻµČēĶ¼ĖłŹ¾£¬Ķ¼ÖŠ”°”±±ķŹ¾ĻąĮ¬µÄĪļÖŹÄÜĻą»„·“Ó¦£¬”°”ś”±±ķŹ¾ÖÖĪļÖŹ×Ŗ»Æ³ÉĮķŅ»ÖÖĪļÖŹ(²æ·Ö·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žŅŃĀŌČ„)”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
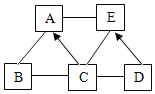
£Ø1£©ĪļÖŹ E ŹĒ_____”£
£Ø2£©Š“³öĻĀĮŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗA+E£ŗ__________£»B+C£ŗ________________”£
£Ø3£©Ķ¼ÖŠĻą»„¹ŲĻµÉę¼°»ł±¾·“Ó¦ĄąŠĶÓŠ_____ÖÖ”£
”¾“š°ø”æFe ![]()
![]() Į½
Į½
”¾½āĪö”æ
AE ĪŖ³õÖŠ»ÆѧĪåÖÖ²»Ķ¬Ąą±šµÄ³£¼ūĪļÖŹ£¬E ĪŖŹĄ½ēÄź²śĮæ×īøߵĽšŹō£¬æÉĶĘ³öEĪŖĢś£¬A ŹĒĻą¶Ō·Ö×ÓÖŹĮæĪŖ160µÄĄ¶É«ČÜŅŗ£¬æÉĶĘ³öAĪŖĮņĖįĶ£¬BÄÜÓėĮņĖįĶ·“Ó¦£¬BŅ²ÄÜÓėC·“Ó¦£¬CÄÜ×Ŗ»ÆĪŖĮņĖįĶ£¬BæÉÄÜĪŖæÉČÜŠŌĒæ¼ī£¬ČēĒāŃõ»ÆÄĘ£¬CŌņĪŖĮņĖį£¬DÄÜÓėĮņĖį·“Ó¦£¬ĒŅDÄÜ×Ŗ»ÆĪŖĢś£¬DæÉÄÜĪŖĢśµÄŃõ»ÆĪļ£¬ČēČżŃõ»Æ¶žĢś£¬“śČėŃéÖ¤£¬·ūŗĻĢāŅā”£
£Ø1£©ĪļÖŹEĪŖĢś£¬»ÆѧŹ½ĪŖ£ŗFe£»
£Ø2£©AĪŖĮņĖįĶ£¬EĪŖĢś£¬ĢśÄÜÓėĮņĖįĶ·“Ӧɜ³ÉĮņĖįŃĒĢśŗĶĶ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ![]() £»
£»
BæÉÄÜĪŖĒāŃõ»ÆÄĘ£¬CĪŖĮņĖį£¬ĒāŃõ»ÆÄĘÓėĮņĖį·“Ӧɜ³ÉĮņĖįÄĘŗĶĖ®£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ![]() £»
£»
£Ø3£©AÓėE·“Ó¦£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦£»
AÓėB·“Ó¦£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
BÓėC·“Ó¦£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
CÓėD·“Ó¦£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
CÓėE·“Ó¦£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦£»
C”śA£ŗ![]() £¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
£¬øĆ·“Ó¦·ūŗĻ”°Į½ÖÖ»ÆŗĻĪļ»„Ļą½»»»³É·ÖÉś³ÉĮķĶāĮ½ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚø“·Ö½ā·“Ó¦£»
D”śE£ŗ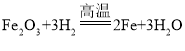 £¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦”£
£¬øĆ·“Ó¦·ūŗĻ”°Ņ»ÖÖµ„ÖŹÓėŅ»ÖÖ»ÆŗĻĪļ·“Ӧɜ³ÉĮķŅ»ÖÖµ„ÖŹŗĶĮķŅ»ÖÖ»ÆŗĻĪļ”±µÄ·“Ó¦£¬ŹōÓŚÖĆ»»·“Ó¦”£
¹ŹĶ¼ÖŠĻą»„¹ŲĻµÉę¼°»ł±¾·“Ó¦ĄąŠĶÓŠĮ½ÖÖ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”抔ĮÖĶ¬Ń§ĻėČ·¶Ø¹¤ŅµŃłĘ·ĮņĖį¼ŲµÄŗ¬Į棬°“Į÷³Ģ½ųŠŠĮĖČēĻĀŹµŃé:
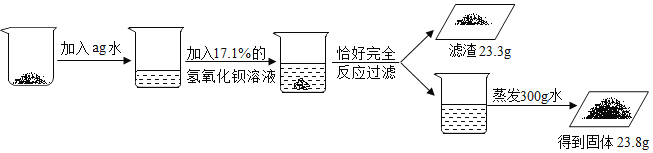
£Ø1£©ĒėŠ“³ö·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½_______£»
£Ø2£©ĮŠ³öĒó½āĮņĖį¼Ų¹ĢĢåÖŹĮæ(x)µÄ±ČĄżŹ½ĪŖ________£»
£Ø3£©¹¤ŅµŃłĘ·ÖŠĮņĖį¼ŲµÄŗ¬ĮæĪŖ______£»
£Ø4£©¼ÓČėĖ®µÄÖŹĮæŹĒ______g£»
£Ø5£©ÓĆ“ĖĮņĖį¼ŲѳʷŗĶĒāŃõ»Æ±µČÜŅŗ·“Ó¦ÖĘĒāŃõ»Æ¼Ų119t£¬ŠčøĆѳʷµÄÖŹĮæĪŖ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉÕ±Ź¢ÓŠŅ»¶ØÖŹĮæµÄĒāŃõ»ÆÄĘŗĶĒāŃõ»Æ¼ŲµÄ¹ĢĢå»ģŗĻĪļ£¬ĻņĘäÖŠ¼ÓČė100 gÖŹĮæ·ÖŹżĪŖ7.3%µÄĻ”ŃĪĖį£¬Ē”ŗĆĶźČ«·“Ó¦£¬µĆµ½109.6 gøĆĪĀ¶ČĻĀµÄ²»±„ŗĶČÜŅŗ”£ŌņŌ¹ĢĢå»ģŗĻĪļÖŠ½šŹōŌŖĖŲµÄÖŹĮæ·ÖŹżÓėĻĀĮŠŹż¾Ż×ī½Ó½üµÄŹĒ
A. 57.5% B. 64.6% C. 67.7% D. 69.6%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»ĢĆ»ÆѧŹµŃéæĪÉĻ£¬ĄĻŹ¦ĪŖĆæ×éĶ¬Ń§·Ö±šĢį¹©ĮĖŅ»ĘæĒāŃõ»ÆÄĘČÜŅŗ£¬ČĆĖūĆĒÓĆ 1%µÄĻ”ŃĪĖįĄ“²ā¶ØĘäČÜÖŹµÄÖŹĮæ·ÖŹż£®ŅŌĻĀŹĒ¼ø×éĶ¬Ń§µÄÉčĻė¼°×ö·Ø£ŗ
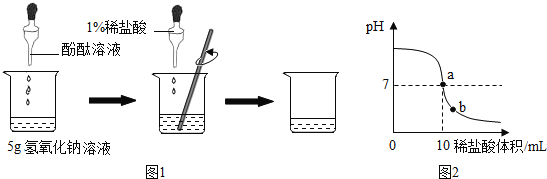
£Ø1£©¼××éĶ¬Ń§µÄŹµŃéČēĶ¼ 1 ĖłŹ¾£ŗŌŚÉÕ±ÖŠ¼ÓČė 5g ĒāŃõ»ÆÄĘČÜŅŗ£¬µĪČė¼øµĪ·ÓĢŖČÜŅŗ£¬ÓƵĪ¹ÜĀżĀżµĪČė 1%µÄĻ”ŃĪĖį£¬²¢²»¶Ļ½Į°č£¬ÖĮČÜŅŗŃÕÉ«Ē”ŗƱäĪŖĪŽÉ«ĪŖÖ¹”£Ēė»Ų“š£ŗ
¢Ł·ÓĢŖČÜŅŗµÄ×÷ÓĆŹĒ_____£»
¢Ś±ßµĪ¼ÓĻ”ŃĪĖį£¬±ßÓĆ²£Į§°ō²»¶Ļ½Į°čµÄÄæµÄŹĒ_____”£
£Ø2£©ŅŅ×éÕūøöŹµŃé¹ż³ĢÖŠČÜŅŗ pH µÄ±ä»ÆĶ¼Ļó£Ø¼ņµ„±ķŹ¾ĪŖĶ¼ 2£©£®Ēė»Ų“š£ŗĶ¼ 2 ÖŠa µć±ķŹ¾µÄŗ¬ŅåŹĒ_____£»b µćČÜŅŗÖŠŗ¬ÓŠµÄŃōĄė×ÓÓŠ_____£ØĢīĄė×Ó·ūŗÅ£©”£
£Ø3£©±ū×éĶ¬Ń§ŌŚµĪ¼ÓĻ”ŃĪĖįŅ»¶ĪŹ±¼äŗ󣬷¢ĻÖČÜŅŗÖŠÓŠÉŁĮæĘųÅŻ²śÉś£®ÕāŅ»”°Ņģ³£ĻÖĻó”±¼¤ĘšĮĖĖūĆĒµÄĢ½¾æÓūĶū£¬ĶعżŹµŃéÖ¤Ć÷£ŗøĆ×éÓƵÄÕāĘæĒāŃõ»ÆÄĘČÜŅŗŅŃ¾²æ·Ö±äÖŹ£®ĒėÓĆ»Æѧ·½³ĢŹ½±ķŹ¾Ęä±äÖŹµÄŌŅņ_____£»ČōŅŖ³żČ„ČÜŅŗÖŠ±äÖŹÉś³ÉµÄŌÓÖŹ£¬Ēė¼ņŅŖŠ“³öÄćµÄŹµŃé·½°ø£ŗ_____”£
£Ø4£©µ±¼××éŌŚ 5g ĒāŃõ»ÆÄĘČÜŅŗÖŠµĪ¼ÓĻ”ŃĪĖį£¬ČÜŅŗīÉ«Ē”ŗƱäĪŖĪŽÉ«Ź±£¬¹²ÓĆČ„ĮĖĻ”ŃĪĖį 7.3g£®¼ĘĖć¼××éÕāĘæĒāŃõ»ÆÄĘČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖ²ā¶ØCuCl2ŗĶFeCl2×é³ÉµÄ»ģŗĻČÜŅŗÖŠFeCl2µÄÖŹĮæ·ÖŹż£¬½ųŠŠČēĻĀŹµŃé:
¢ŁČ”200g»ģŗĻČÜŅŗ¼ÓČė×ćĮæµÄAgNO3ČÜŅŗ£¬¾¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘĮ棬µĆµ½143. 5gAgCl¹ĢĢå;
¢ŚĮķČ”Ō»ģŗĻČÜŅŗø÷200gÓėŗ¬ÓŠŌÓÖŹµÄ·ĻĢśŠ¼·“Ó¦(ŌÓÖŹ²»ČÜÓŚĖ®£¬Ņ²²»²ĪÓė·“Ó¦)£¬¹²×öĮĖĪå×鏵Ń飬Ę䏵Ń鏿¾ŻČēĻĀ±ķ”£
ŹµŃé×鱚 | Ņ» | ¶ž | Čż | ĖÄ | Īå |
»ģŗĻČÜŅŗÖŹĮæ/g | 200 | 200 | 200 | 200 | 200 |
ĢśŠ¼ÖŹĮæ/g | 6 | 9 | 12 | 15 | 18 |
Īö³öĶµÄÖŹĮæ/g | 6.4 | 9.6 | m | 16 | 16 |
Ēė·ÖĪö¼ĘĖć:
£Ø1£©±ķÖŠµŚČż×鏵ŃéµÄmÖµĪŖ____________”£
£Ø2£©µŚ___________×鏵ŃéĒ”ŗĆĶźČ«·“Ó¦”£
£Ø3£©Ō»ģŗĻČÜŅŗÖŠFeCl2µÄÖŹĮæ·ÖŹżĪŖ_________? (¼ĘĖć½į¹ū¾«Č·µ½ 0.1%)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒČÕ³£Éś»īÖŠ³£ÓƵēņ»š»śŹ¾ŅāĶ¼£¬ Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
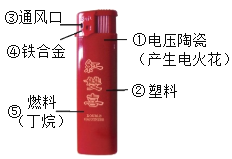
£Ø1£©Ķ¼Ź¾ÖŠŹōÓŚ½šŹō²ÄĮĻµÄŹĒ______£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£»ŹōÓŚÓŠ»śŗĻ³É²ÄĮĻµÄŹĒ________”£
£Ø2£©“ņ»š»śČ¼ĮĻµÄÖ÷ŅŖ³ÉŹĒ¶”Ķé£ØC4H10£©£¬Š“³ö¶”ĶéČ¼ÉյĻÆѧ·½³ĢŹ½_______________”£
£Ø3£©¶”ĶéŌŚĶس£×“æöĻĀ³ŹĘųĢ¬£¬ ÓŠ“Ģ¼¤ŠŌĘųĪ¶”£“ņ»š»śÅ¼¶ūĪ““ņ×ÅŹ±»įĪŵ½Ņ»ÖÖ“Ģ¼¤ŠŌĘųĪ¶£¬ ĖµĆ÷_____________________£Ø“Ó·Ö×ӵĽĒ¶Č·ÖĪö)”£
£Ø4£©“ņ»š»śŹ¹ÓĆ½įŹųŹ±ĖÉæŖČ¼ĮĻ·§£¬ “ņ»š»ś¾Ķ»įĻØĆš£¬ “ĖĆš»š·½·ØŅĄ¾ŻµÄŌĄķŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫Ļ”ŃĪĖįĀżĀżµĪČė×°ÓŠĒāŃõ»ÆÄĘČÜŅŗµÄÉÕ±ÖŠ£¬ÓĆĪĀ¶Č¼Ę²ā³öÉÕ±ÖŠČÜŅŗµÄĪĀ¶Č£¬ČÜŅŗĪĀ¶ČĖę¼ÓČėĻ”ŃĪĖįµÄÖŹĮæ¶ų±ä»ÆČēĶ¼ĖłŹ¾£ŗ
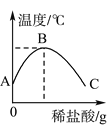
(1)ÓÉĶ¼æÉÖŖ£¬Ļ”ŃĪĖįÓėĒāŃõ»ÆÄĘČÜŅŗ·¢ÉśµÄ·“Ó¦ŹĒ________(Ģī”°·ÅČČ”±»ņ”°ĪüČČ”±)·“Ó¦”£
(2)“ÓAµ½B¹ż³ĢÖŠ£¬ÉÕ±ÖŠČÜŅŗµÄpHÖš½„________”£
(3)______µćŹ±Ē”ŗĆĶźČ«·“Ó¦£¬CµćµÄČÜŅŗÖŠŗ¬ÓŠµÄČÜÖŹĪŖ________”£
(4)ČēĶ¼ŹĒĒāŃõ»ÆÄĘČÜŅŗÓėĻ”ŃĪĖįĒ”ŗĆĶźČ«·“Ó¦µÄĪ¢¹ŪŹ¾ŅāĶ¼£¬
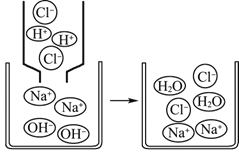
ÓÉ“ĖµĆ³öøĆ·“Ó¦µÄŹµÖŹŹĒ____”£Š“³öĮķŅ»øö·ūŗĻøĆ·“Ó¦ŹµÖŹµÄ»Æѧ·½³ĢŹ½______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤Ņµ²śĘ·¹żŃõ»ÆøĘ¾§Ģå£ØCaO2”¤8H2O£©½ĻĪČ¶Ø£¬³Ź°×É«£¬Ī¢ČÜÓŚĖ®£¬¹ć·ŗÓĆÓŚ»·¾³É±¾ś”¢Ļū¶¾”£ŅŌ±“æĒ£ØÖ÷ŅŖ³É·ÖŹĒ CaCO3£¬ŌÓÖŹ²»²Ī¼Ó·“Ó¦Ņ²²»ČÜÓŚĖ®£©ĪŖŌĮĻÖʱø CaO2µÄĮ÷³ĢČēĻĀ£ŗ
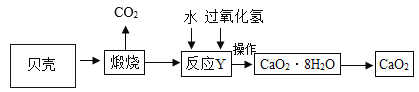
£Ø1£©CaO2ÖŠŃõŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ___________£»
£Ø2£©ÉĻŹöĮ÷³ĢÖŠ½«¹żŃõ»ÆøĘ¾§Ģå“ÓČÜŅŗÖŠ·ÖĄėµÄ²½ÖčŹĒ¹żĀĖ£¬øĆ²Ł×÷ÖŠÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ²£Į§°ō”¢ ÉÕ±ŗĶ_______________£¬ĘäÖŠ²£Į§°ōµÄ×÷ÓĆŹĒ_______________£»
£Ø3£©·“Ó¦ Y ŠčŅŖŌŚµĶĪĀĢõ¼žĻĀ½ųŠŠ£¬ĘäŌŅņŹĒ_________________£»
£Ø4£©»ńČ”µÄ CaO2 ÖŠ³£ŗ¬ÓŠ Ca(OH)2 ŌÓÖŹ£¬ŌŅņŹĒ_______________(ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ¼ÓČė X ČÜŅŗ²¢²åČėĪĀ¶Č¼Ę£¬ÖšµĪ¼ÓČėĮņĖįČÜŅŗ£¬¹Ū²ģµ½ŗģÉ«ĶŹČ„£¬ĪĀ¶Č¼ĘŹ¾ŹżÉĻÉż”£Ö¤Ć÷¼īÓėĖįÄÜ·¢Éś·“Ó¦£¬ĒŅ·Å³öČČĮ攣
£Ø1£©¼ÓČėµÄ X ČÜŅŗÓ¦øĆŹĒ_____ČÜŅŗ£»
£Ø2£©¼×Ķ¬Ń§Ģį³öµĪČėµÄĮņĖį²»ÄÜÓĆÅØĮņĖį£¬ĖūµÄĄķÓÉŹĒ_____£»
£Ø3£©ŅŅĶ¬Ń§Ģį³öŗģÉ«ĶŹČ„²»ÄÜĖµĆ÷ĖįŗĶ¼īĒ”ŗĆ·“Ó¦ĶźČ«£¬ĪŖĮĖÖ¤Ć÷ŹĒ·ńĒ”ŗĆ·“Ó¦£¬æÉČ”ÉĻŹö·“Ó¦ŗóµÄĪŽÉ«ČÜŅŗÉŁŠķ¼ÓČė_____¼“æÉ£ØĢīŠņŗÅ£©”£
¢ŁĶ ¢ŚĆ¾ ¢ŪŃõ»ÆĶ ¢ÜBaCl2 ČÜŅŗ ¢ŻNa2CO3 ČÜŅŗ
£Ø4£©ČōČ”10%µÄĒāŃõ»ÆÄĘČÜŅŗ100gŗĶ10%µÄĮņĖįČÜŅŗ100g»ģŗĻŗ󣬼ÓČė×ĻÉ«ŹÆČļ£¬Ōņ“ĖŹ±ČÜŅŗ³Ź_____É«£ØĢīŠņŗÅ£©”£
¢Ł×Ļ ¢Śŗģ ¢ŪĄ¶
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com