
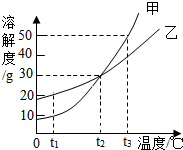
 如图是甲、乙两种固体物质的溶解度曲线.t1℃时,将5g乙加到10g水中可得到12g溶液;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲;将t3℃时150g甲的饱和溶液稀释为20%,需加水100g.
如图是甲、乙两种固体物质的溶解度曲线.t1℃时,将5g乙加到10g水中可得到12g溶液;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲;将t3℃时150g甲的饱和溶液稀释为20%,需加水100g. 分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;t1℃时,乙的溶解度是20g,将5g乙加到10g水中可得到=2g+10g=12g;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲,因为甲的溶解度随温度的升高变化比乙大;将t3℃时,甲的溶解度是50g,把150g甲的饱和溶液稀释为20%,设需加水的质量为x,$\frac{50g}{150g+x}×100%=20%$,x=100g.
解答 解:t1℃时,乙的溶解度是20g,将5g乙加到10g水中可得到=2g+10g=12g;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲,因为甲的溶解度随温度的升高变化比乙大;将t3℃时,甲的溶解度是50g,把150g甲的饱和溶液稀释为20%,设需加水的质量为x,$\frac{50g}{150g+x}×100%=20%$,x=100g;故答案为:12;甲;100;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碘酒是混合物-由不同种分子构成 | |
| B. | 气体受热膨胀-温度升高,分子自身体积变大 | |
| C. | 过氧化氢溶液加入二氧化锰能生成氧气,水中加入二氧化锰不能生成氧气-不同分子,性质不同 | |
| D. | 瓜果飘香-分子在不停地运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)查看答案和解析>>
科目:初中化学 来源: 题型:推断题
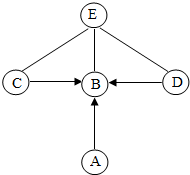 如图中A、B、C、D、E是初中化学中常见的物质,B、C、D、E是不同类别的无机化合物,且它们都含有同一种元素,已知A为红色固体,D可以用于除去铁锈,“-”表示物质在一定条件下可以发生化学反应,“→”表示在一定条件下一种物质可以转化成另一种物质,五种物质的关系如下:
如图中A、B、C、D、E是初中化学中常见的物质,B、C、D、E是不同类别的无机化合物,且它们都含有同一种元素,已知A为红色固体,D可以用于除去铁锈,“-”表示物质在一定条件下可以发生化学反应,“→”表示在一定条件下一种物质可以转化成另一种物质,五种物质的关系如下:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com