


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
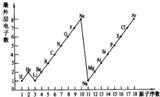 19、图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
19、图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:
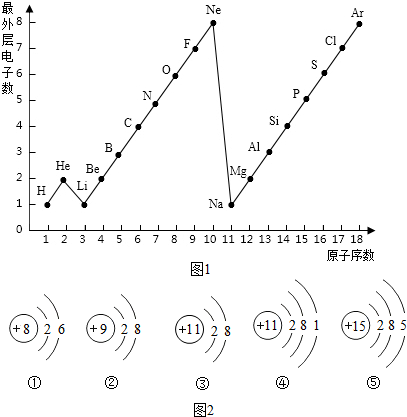
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.
已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快.查看答案和解析>>
科目:初中化学 来源: 题型:
 图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:
图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com