
分析 (1)根据电解水的反应几轮等分析回答;
(2)根据水的污染源和净化水的措施分析回答.
解答 解:(1)水通电分解生成了氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,由此可证明水是由氢、氧元素组成的.
(2)水体污染的来源主要有工业污染、生活污染和农业污染.可以采用多种方法净水,净化程度最高的方法是蒸馏,蒸馏得到的水是纯水.
故答为:(1)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,氢、氧.(2)生活,农业,蒸馏.
点评 本题主要考查了水的组成、污染源和净化等的知识,属于基础的知识,根据已有的知识分析解答即可.


科目:初中化学 来源: 题型:实验探究题
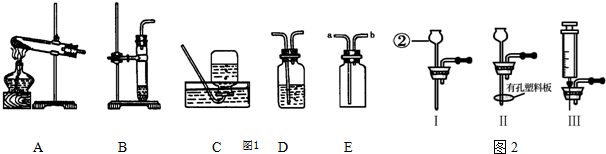
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
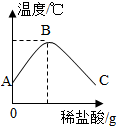 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示:
将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
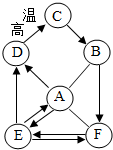 A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).
A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 试验编号 | 盐酸的质量分数/% | 反应温度 | 铝丝消失时间/s |
| ① | 3 | 20 | 500 |
| ② | 6 | 20 | 300 |
| ③ | 6 | 30 | 80 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com