
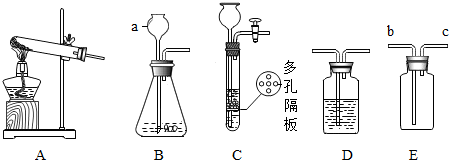
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,采用的方法只要能使试管内体积膨胀就可以了,氧气有助燃性进行分析;
(3)根据该装置可以利用气体的压强将固体和液体分离进行分析;
(4)根据高锰酸钾具有强氧化性进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,采用的方法只要能使试管内体积膨胀就可以了,所以采用的方法有:用热毛巾包捂或用酒精灯微热,氧气有助燃性,所以具体的验满方法是:将带火星的木条伸到c导管口,木条复燃,证明集满;
(3)该装置可以利用气体的压强将固体和液体分离,所以具有的优点是:可以控制反应的发生和停止;
(4)高锰酸钾具有强氧化性,所以高锰酸钾会将二氧化硫氧化,现象为:溶液由紫红色变为无色或褪色.
故答案为:(1)长颈漏斗;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用热毛巾包捂或用酒精灯微热;将带火星的木条伸到c导管口,木条复燃,证明集满;
(3)控制反应的发生和停止;
(4)溶液由紫红色变为无色或褪色.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液 | |
| B. | 金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2 | |
| C. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| D. | 因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰 不锈钢 天然气 | B. | 二氧化锰 金刚石 生铁 | ||
| C. | 酒精 生石灰 葡萄糖 | D. | 氢氧化钠 铁 冰水共存物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
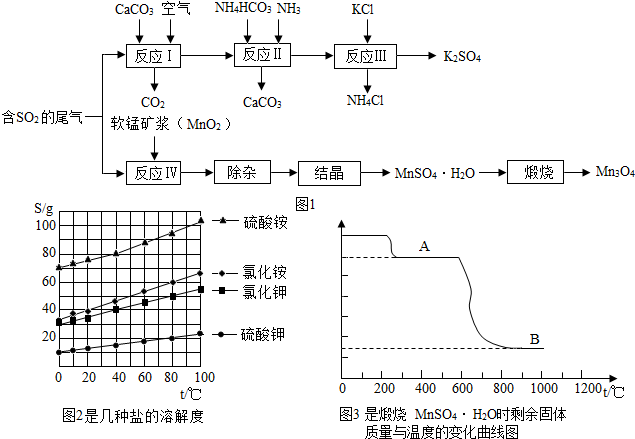
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 反应② 实验现象 | 结论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想1不成立 |
| ②用试管取少量KCl溶液,滴入1-2滴无色酚酞试液 | 试管内溶液不变色 | 猜想2不成立 |
| ③用试管取少量KOH溶液,滴入1-2滴无色酚酞试液 | 试管内溶液变红 | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 土笋冻--补充蛋白质 | B. | 鱿鱼--用甲醛保鲜 | ||
| C. | 海蛎煎--补锌和钙 | D. | 馅饼--制作时,加小苏打有利发酵 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | S | B. | SO2 | C. | SO3 | D. | CO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
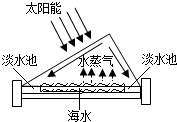 水是生命之源,“爱惜水、保护水”是每个公民的义务和责任.
水是生命之源,“爱惜水、保护水”是每个公民的义务和责任.| 试剂 现象 污水 | 石蕊试液 | 氯化钡溶液 |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com