
分析 (1)根据苹果酸的化学式为C4H6O5进行分析;
(2)利用相对原子质量之和等于相对分子质量解决;
(3)元素的质量比等于相对原子质量和的比;
(4)元素的质量分数=$\frac{该元素的相对原子质量之和}{相对分子质量}$×100%;
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)已知苹果酸的化学式为C4H6O5,则每个分子中含4+6+5=15个原子;
(2)相对原子质量之和等于相对分子质量,所以苹果醋的相对分子质量是12×4+6×1+16×5=134;
(3)元素的质量比等于相对原子质量和的比,所以苹果醋中C、H、O三种元素的质量比是(12×4):(6×1):(16×5)=24:3:40;
(4)苹果酸中碳元素的质量分数=$\frac{12×4}{134}×100$%=35.8%.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,则67克苹果酸中含碳元素的质量为:67g×$\frac{12×4}{134}×100$%=24g.
故答案为:
(1)15;(2)134;(3)24:3:40;(4)35.8%.(5)24.
点评 解答时正确利用苹果酸的化学式和名称,利用化学式提供的信息,然后结合学过的知识来解答问题.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:初中化学 来源: 题型:解答题
 医生给病人输液时,常用葡萄糖注射液.右图为葡萄糖注射液的部分标签图,根据如图 回答下列问题:
医生给病人输液时,常用葡萄糖注射液.右图为葡萄糖注射液的部分标签图,根据如图 回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 密度/g/cm3 | 1.07 | 1.14 | 1.30 | 1.50 | 1.73 | 1.84 |
| 溶质质量分数/ | 10 | 20 | 40 | 60 | 80 | 98 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 部分结冰的蒸馏水 | B. | “农夫山泉”矿泉水 | ||
| C. | 雨后清新的空气 | D. | 用KMnO4制取O2后剩余的固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 同种分子构成的物质一定是纯净物 | |
| B. | 含氧元素的化合物不一定是氧化物 | |
| C. | 同种元素组成的物质一定是单质 | |
| D. | 不同种元素组成的纯净物一定是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
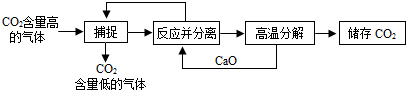
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com