
 某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.
某补钙剂说明书的部分信息如图所示,现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸反应),恰好完全反应后称得剩余物的质量为55.6g.分析 (1)根据缺钙会引起骨质疏松、佝偻病解答;
(2)根据质量守恒分析二氧化碳的质量,根据二氧化碳的质量结合化学方程式可以计算出碳酸钙的质量即可解答;
(3)根据二氧化碳的质量结合化学方程式可以计算出HCl的质量即可解答.
解答 解:(1)缺钙老年人会引起骨质疏松、青少年会患佝偻病.
(2)根据质量数恒定律,生成二氧化碳的质量为20g+40g-55.6g=4.4g
设20片该药剂中含CaCO3的质量为x,40g盐酸中含HCl的质量为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 4.4g
$\frac{100}{y}=\frac{73}{y}=\frac{44}{4.4g}$
x=10g y=7.3g
(2)每片含CaCO3的质量为$\frac{10g}{20}$=0.5g
(3)该盐酸中溶质的质量分数是7.3g÷40g×100%=18.3%
答:(1)佝偻病;(2)该品牌补钙药剂每片含CaCO3的质量为0.5g;(3)该盐酸中溶质的质量分数为18.3%.
点评 本题主要考查学生运用化学方程式进行和质量分数公式进行计算的能力.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:实验探究题
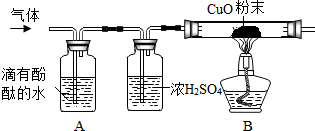
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
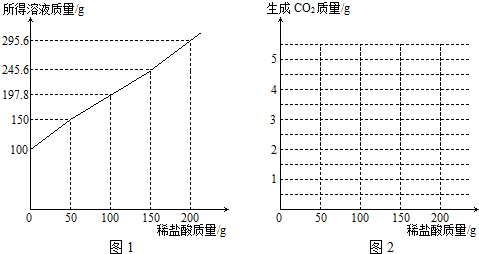
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
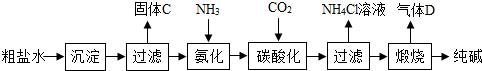
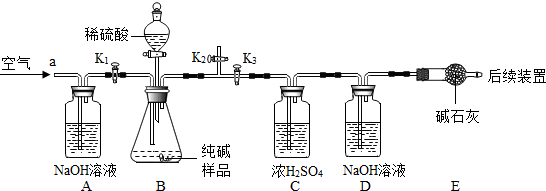
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+ | |
| B. | 滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Mg2+ | |
| C. | 滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+ | |
| D. | 滤纸上有Ag、Cu、Zn、Mg,滤液中有Mg2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则四种说法正确的个数为( )
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则四种说法正确的个数为( )| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 在实验中经常出现实验现象与理论的“不配合”,理性思考这些现象有助于提高我们的科学素养.
在实验中经常出现实验现象与理论的“不配合”,理性思考这些现象有助于提高我们的科学素养.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙醇属于可再生能源 | |
| B. | “可燃冰”将成为未来的新能源 | |
| C. | 将煤碳加工成蜂窝煤,能使煤燃烧更充分 | |
| D. | 化学电池是将化学能传化为热能的一种方式 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com