

| A. | 图1中乙溶液一定不饱和 | |
| B. | 图2中两溶液中溶质质量分数一定相等 | |
| C. | 图3中N表示甲的溶解度曲线 | |
| D. | 图2中两溶液降温至30℃一定都不会析出晶体 |
分析 A、图1中乙无溶质剩余,无法判断是否是饱和溶液;
B、图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,并结合溶质的质量分数的计算公式完成解答;
C、图1中20℃时,将等质量的甲、乙两种固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,甲有固体剩余,说明甲的溶解度小于乙,结合图3完成解答;
D、根据图3可知两种物质的溶解度都随温度升高而增大,因此30℃时,甲乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等;再根据图1中信息可以知道20℃时乙中没有晶体析出进行解答.
解答 解:A、图1中乙无溶质剩余,无法判断是否是饱和溶液,故A错误;
B、图2中均无固体剩余,说明全部溶解,相同质量的溶剂溶解了相同质量的溶质,结合溶质的质量分数的计算公式可以知道,它们形成的溶液中溶质的质量分数也相等,故B正确;
C、根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故N表示的是乙物质的溶解度曲线,故C错误;
D、根据图3可知两种物质的溶解度都随温度升高而增大,因此30℃时,甲乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等;再根据图1中信息可以知道20℃时乙中没有晶体析出,因此30℃时乙中一定也无晶体析出,因此图2中两溶液降温至30℃一定都不会析出晶体,故D正确.
故选:BD.
点评 本题首先要熟记和理解固体溶解度曲线及其使用,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或图表信息,结合所学的相关知识和技能按照题目的要求,认真地进行选择或解答即可.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 项目 | 内容 |
| A | 化学反应基本类型 | ①化合反应4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 ②分解反应H2CO3═H2O+CO2↑ ③置换反应C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ ④复分解反应HCl+NaOH═NaCl+H2O |
| B | 化学与生活 | ①除去餐具油污--用洗洁精乳化 ②人体缺乏维生素A--引起夜盲症 ③干冰--用于人工降雨 ④鉴别羊毛和合成纤维--点燃后闻气味 |
| C | 化学实验数据记录 | ①用10mL量筒量取7.25mL水 ②用pH试纸测得苹果汁的pH为3.2 ③用托盘天平称取5.6g铁粉 |
| D | 化学中常见的“三” | ①煤、石油、天然气--三大化石燃料 ②塑料、合成纤维、合成橡胶--三大合成材料 ③分子、原子、离子--构成物质的三种粒子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 目前计入空气质量日报污染指数的项目包括CO2 | |
| B. | 空气质量级别越高,空气质量越好 | |
| C. | 空气中O2的质量分数约为21% | |
| D. | 分离液态空气可制得无色氮气和淡蓝色的液态氧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大力宣传新《环保法》等法律法规,推进生态文明建设 | |
| B. | 太湖、阳澄湖等湖泊减少围网养殖 | |
| C. | 实行垃圾分类回收,禁止向河道倾倒垃圾 | |
| D. | 餐馆洗菜、洗碗水直接排入马路上的雨水窨井 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
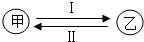 化学变化中,同种元素可在不同物质中“旅行”.
化学变化中,同种元素可在不同物质中“旅行”.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

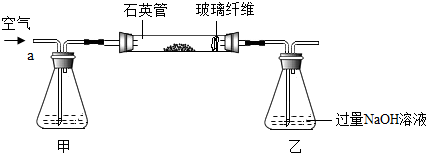
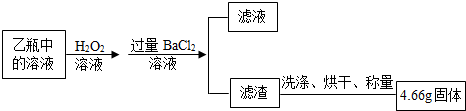
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制取气体时,先装药品,后检查装置的所密性 | |
| B. | 稀释浓硫酸时,先把浓硫酸倒入烧杯,后加水并用玻璃棒不断搅拌 | |
| C. | 用托盘天平称量药品时,先调节天平平衡,后称量 | |
| D. | 木炭还原氧化铜结束时,先停止加热,后把导管从盛有石灰水的试管中取出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com