
| A. | 生成水、气体或沉淀的反应一定都是复分解反应 | |
| B. | 稀盐酸和稀硫酸的化学性质完全相同 | |
| C. | 一种物质的饱和溶液一定比不饱和溶液浓度大 | |
| D. | 合金的组成中一定有金属元素 |
分析 A、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应.
B、根据稀盐酸和稀硫酸的化学性质,进行分析判断.
C、根据溶液是否饱和与溶质质量分数的关系,进行分析判断.
D、根据合金的特征,进行分析判断.
解答 解:A、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应,生成水、气体或沉淀的反应不一定都是复分解反应,如CO2+Ca(OH)2═CaCO3↓+H2O,故选项推理错误.
B、稀盐酸和稀硫酸的化学性质不完全相同,如稀硫酸能与氯化钡溶液反应,而稀盐酸不能,故选项推理错误.
C、一种物质的饱和溶液不一定比不饱和溶液浓度大,如0℃时硝酸钾的饱和溶液不一定比60℃时硝酸钾的不饱和溶液浓,故选项推理错误.
D、合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金具有以下特点:①一定是混合物;②合金中至少有一种金属等,故选项推理正确.
故选:D.
点评 本题难度不大,掌握复分解反应的特征、酸的化学性质、溶液是否饱和与溶质质量分数的关系、合金的特征等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 用碳酸氢钠治疗胃酸过多 | B. | 用金刚石做玻璃刀的刀头 | ||
| C. | 用石墨做铅笔芯写字 | D. | 用钨做电灯泡里的灯丝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
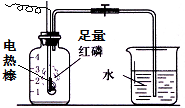 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用滴管滴加液体时,将滴管伸入试管中 | |
| B. | 用量筒量取7mL液体时,最好选用10mL量筒 | |
| C. | 检验一集气瓶中是否集满氧气,可以将带火星的木条伸入集气瓶中 | |
| D. | 给试管里的液体加热时,试管底部要与酒精灯芯接触 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
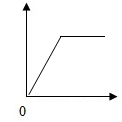 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 序号 | 横坐标 | 纵坐标 |
| A | 向一定量稀硫酸中加入锌粉的质量 | 溶液中氢元素的质量 |
| B | 向一定量的澄清石灰水中加入 碳酸钠溶液的质量 | 产生沉淀的质量 |
| C | 向一定量的硫酸和硫酸镁的混合 溶液中加入氢氧化钡溶液 | 生成氢氧化镁的质量 |
| D | 在一定温度下,向一定量不饱和硝 酸钾溶液中加入硝酸钾固体的质量 | 溶液中溶质的质量分数 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
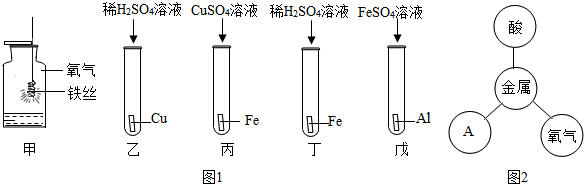
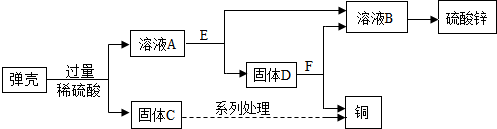
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 解:68g过氧化氢中氧元素的质量为:68g×$\frac{20}{{H}_{2}{O}_{2}}$×100%=68g×$\frac{32}{34}$=64g,因为 氧气中的氧元素来自于过氧化氢,所以68g过氧化氢产生氧气的质量为64g. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com