
【题目】赶走雾霾,让蓝天永驻,对汽车尾气的净化是必要的.如图是某种汽车尾气净化装置里的微观反应过程,该反应需要在一种“铂催化剂”的催化下进行,则下列说法正确的是
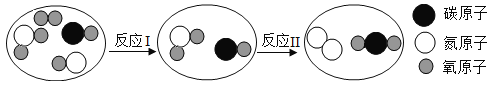
A.反应前后分子改变,原子不变
B.该反应中各物质均为化合物
C.铂催化剂在反应结束后质量改变
D.反应Ⅱ为置换反应
 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:
【题目】研究金属的腐蚀对资源的利用和保护意义重大。
(1)为了探究铁锈蚀的条件,进行如图 1 所示实验。
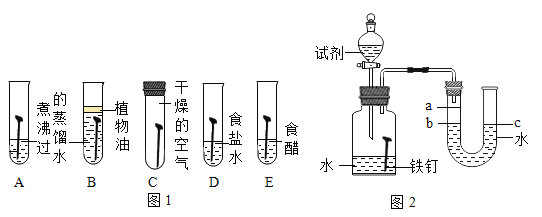
①通过观察实验 A、B、C 中的现象,经过科学严谨的推理得出结论:铁锈蚀是铁与____________发生化学反应的过程。
②实验 D 和 E 的目的是进一步探究铁在盐溶液和酸的环境中是否更容易锈蚀。铁跟醋酸(CH3COOH) 反 应生成醋酸亚铁[ (CH3COO)2Fe ]和氢气 ,请写出反应的化学方程式____________________。
(2)家中的刀具若沾有食盐水锈蚀更快。为了进一步探究影响铁锈蚀速率的因素,做了如下的实验。
(提出问题)铁锈蚀速率与哪些因素有关。
(查阅资料)氯化钠溶液能导电;乙醇溶液不能导电。
(猜想假设)铁的锈蚀速率与下列因素有关:
I._________________;
II.氧气的含量;
Ⅲ.水溶液的导电性。
(实验探究)每次取两套如图 2 所示的装置,编号为甲、乙。向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致)。
影响 因素 | 实验设计 | 实验现象 | 实验结论及解释 |
I. | 装置甲放入 25℃恒温环境中, 装置乙放入 40℃恒温环境中。 | 两套装置中铁钉均锈蚀,且 U型管中液面均由 b 处上升至 a处,所需时间甲>乙 | ____________ |
II. | 在相同温度下,向甲、乙两套装置的集气瓶中分别通入氧气和空气。 | 铁钉均锈蚀,且 U 型管中液面由 b 处上升至 a 处,所需时间甲___________乙 | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快。 |
Ⅲ. | ______________________ | 两套装置中铁钉均锈蚀,且 U 型管中液面均由 b 处上升至 a 处,所需时间甲<乙 | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,铁的锈蚀速率加快。 |
(反思与提高)根据该探究实验以及你所学的知识,判断下列说法正确的是___________(填序号)。
A 金属的腐蚀是指金属单质与其它物质发生化学反应的过程
B 金属腐蚀不一定要有氧气参加
C 金属越活泼,就越容易被锈蚀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CaO和NaOH固体的混合物,俗名“碱石灰”,实验室常用作干燥剂.碱石灰在空气久置会吸收空气中的水和二氧化碳而变质.某实验小组为确定一瓶久置的碱石灰样品的成分,设计了图所示实验流程.
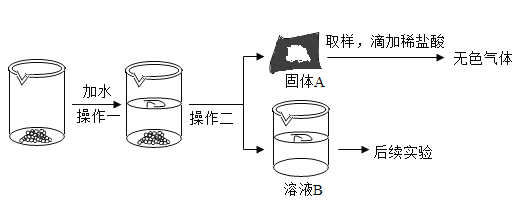
请你参与探究过程:
(1)为了使样品充分溶解,操作一中还要用到的玻璃仪器是__;操作二的名称是__.
(2)固体A中一定含有__.
(3)溶液B成分的探究.
(查阅资料)
①Ca(OH)2、Na2CO3溶于水无明显的温度变化;
②Na2CO3溶液呈碱性,能使酚酞试液变红;
③CaCl2溶液呈中性且能与碳酸钠发生复分解反应.
(猜想)溶液B中溶质可能为:①NaOH ②Na2CO3③NaOH和Na2CO3④Ca(OH)2和__
(设计方案并进行实验)甲、乙同学分别设计如下方案并进行探究:
甲同学:取少量溶液B于试管中,滴加足量的稀盐酸,产生大量气泡,则溶液B中的溶质是Na2CO3.
乙同学:取少量溶液B于试管中,滴加几滴酚酞试液,溶液变成红色,则溶液B中的溶质一定含有NaOH.丙同学认真分析上述二位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断.他认为B溶液中一定含有Na2CO3,可能含有NaOH.为进一步确认溶液B中是否含NaOH,他做了如下实验.
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,在滤液中滴加酚酞试液 | __ | 猜想③正确 |
实验步骤①的目的是__.
(4)实验过程中,同学们发现向样品中加水时还放出大量的热.综合以上探究,下列对样品成分分析正确的是__(填序号).
A 一定有
B 一定有Na2CO3
C 一定有CaO
D 至少有NaOH、CaO中的一种.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示装置回答有关问题:
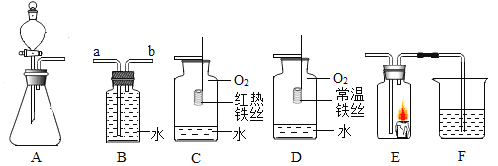
(1)装置 A 的优点是_________。
(2)若用装置 B 排水法收集氧气,气体从______________(填“a”或“b”)端导管通入瓶内。
(3)对比装置 C 和 D,可以得出可燃物燃烧的条件是______________。
(4)某同学连接 A、E、F 进行实验,A 中所加药品不同,F 中所加药品相同。
①若实验时 E 中蜡烛熄灭,F 中溶液变浑浊,则 A 中反应的化学方程式为______________;
②若实验时 E 中蜡烛燃烧更旺,F 中溶液变浑浊,则 A 中反应的化学方程式为______________;
③实验时 F 中溶液的作用是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】被誉为“中国天眼”的FAST,是目前世界上最大单口径,最灵敏的射电望远镜,2016年9月在贵州落成.如图所示,请完成下列各题
(1)望远镜搭架所用的材料是角钢,角钢中含有的非金属元素是:____(填一种即可),选择角钢而不用纯铁做搭架的主要原因是:______
(2)角钢中含有锰和硅,锰可以与稀盐酸反应,生成锰的化合物中锰元素显+2价.请你试着写出锰与稀盐酸反应的化学方程式 :_____
(3)请你写出一条防止铁制材料生锈的具体措施:___铝有很好的抗腐蚀性,是因为铝在空气中易与氧气反应生成致密的:_______(填化学式)薄膜.

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】皮肤受到蚊虫叮咬,十分痒痛,资料显示原来是蚊虫分泌出的蚁酸所致。某兴趣小组的同学决定对蚁酸进行一翻研究。
(提成问题)蚁酸的成分是什么?它有什么性质?
(查阅资料)蚁酸一般指甲酸,无色且有刺激性气味的液体。化学式为HCOOH,在一定的条件下能分解成两种氧化物。
(探究1)测定蚁酸溶液的pH__7(填“>”或“<”),说明蚁酸溶液呈酸性。
(探究2)(1)甲同学根据蚁酸中含有____元素推断蚁酸分解的生成物中有水。
(2)蚁酸分解生成的另一种气体是氧化物,乙同学提出两种猜想:
假设1:该气体是____; 假设2:该气体是CO。
(实验验证)如图
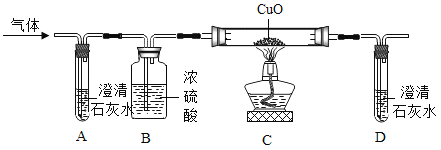
(3)如果A试管中的澄清石灰水变浑浊,证明假设__成立。
(4)如果假设2成立,C装置硬质玻璃管中的现象为___。
(讨论交流)(5)丙同学质疑,仅仅通过C装置中的实验现象,不能证明假设2成立,你支持他的观点吗?____(填“支持”或“不支持”),理由是__。
(6)丁同学发现该实验装置有一个明显的缺陷:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是以实验为基础的科学,请回答下列问题。
(1)下图是实验室中常用到的仪器,现用H2O2溶 液和MnO2来制取氧气。
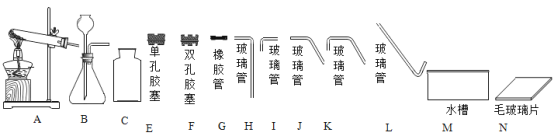
①该反应的化学方程式是____________,MnO2在反应中起的是______________作用;
②若用排水法收集氧气,除选用B装置外,还应该选择所给仪器中的F、I、K、M、N和_______________。
(2)化学兴趣小组的同学按图操作,测定实验室中部分变质的NaOH固体中Na2CO3的质量分数。
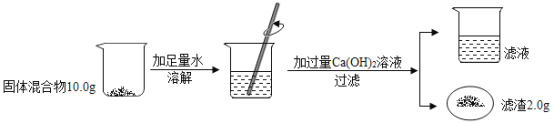
分析题中信息,可知发生反应的化学方程式为:![]() ,则所得滤液中的溶质是_______________。通过相关计算可知,部分变质的NaOH固体混合物中含Na2CO3的质量分数为_______________。
,则所得滤液中的溶质是_______________。通过相关计算可知,部分变质的NaOH固体混合物中含Na2CO3的质量分数为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化锰和过氧化氢酶均能催化过氧化氢分解制取氧气。为比较两者的催化能力,小明按图甲所示装置进行了如下实验。
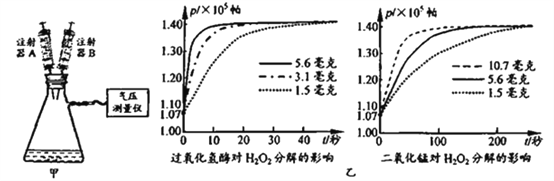
①取1.5毫克过氧化氢酶和8毫升蒸馏水加入容器中,搅拌后塞紧橡皮塞。
②用注射器A从容器中抽出2毫升气体,用注射器B将2毫升H2O2溶液注入容器中,采集数据.直至反应结束。
③用3.1毫克、3.6毫克过氧化氢酶及1.5毫克、5.6毫克、10.7毫克二氧化锰重复上述实验,获取数据如图乙。
(1)步骤②将注射器B中的2mL H2O2溶液全部注入容器前,用注射器A先从容器中抽出2毫升气体,其目的是__________。
(2)小明分析相关数据,得出“过氧化氢酶对过氧化氢的催化能力比二氧化锰强”这一结论,其依据是_____________。
(3)查阅资料得知:过氧化氢分解为放热反应。小明推测:过氧化氢酶质量过大,可能导致实验过程中过氧化氢分解突然变慢。请说明其理由:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
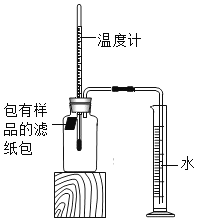
【题目】小明对铁的锈蚀进行如下探究.室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图.观察到量筒内水沿导管慢慢进入净容积为146mL的广口瓶.当温度恢复至室温,且量筒内水面高度不再变化时读数.记录量筒起始和最终的读数以及所需时间如下表.
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
① | 1g铁粉、0.2g碳和10滴水 | 100 | 78 | 约120 |
② | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 78 | 约70 |
③ | / | / | / |
(1)实验①和②说明NaCl可以__ (填“加快”或“减慢”)铁锈蚀的速率.
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是__ (填“放热”或“吸热”)过程.
(3)实验后滤纸包中生成的新物质主要成分的化学式:__.
(4)实验①和③是探究碳对铁锈蚀速率的影响,填写实验③的样品组成:__.
(5)小明认为该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是__%(得数保留3位有效数字).
(6)为进一步验证(5)小题的实验结果,现仅提供:量筒、大烧杯、玻璃棒、水、滤纸包(内含铁粉、碳、水和NaCl),请你帮助小明再设计一个测量空气中氧气体积含量的实验方案______(可画简图表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com