
【题目】将53克的碳酸钠溶液与克74克氯化钙溶液混合,两物质恰好完全反应,生成沉淀,过滤,所得滤液的质量为117克,
(反应的化学方程式:Na2CO3 + CaCl2 == CaCO3↓+2NaCl)
试计算:(1)反应后生成的沉淀质量为_______ g
(2)所得滤液中溶质的质量分数为_______________?
科目:初中化学 来源: 题型:
【题目】不含结晶水的甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是
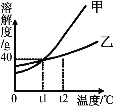
A. t1℃时,甲、乙饱和溶液中含溶质的质量相等
B. t1℃时,甲、乙两种物质各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g
C. t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D. t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测得工业纯碱中碳酸钠的质量分数(常含少量NaCl),小明同学设计的实验装置如图甲,准确称取一定量的纯碱样品,从分液漏斗中滴入稀硫酸。已知碱石灰既能吸收水也能吸收二氧化碳。

(1)图甲中仪器a内发生的化学方程式为______________________。
(2)小红觉得小明的实验装置会导致较大的误差,故设计了图乙的装置,请你写出图乙装置的优势(写出两点即可):_________________、______________。
(3)小红用图乙装置进行实验,步骤为:①准确称取盛有碱石灰的干燥管的质量为158.0 g,再准确称取11.0 g纯碱样品并全部放入A中;②组装全部反应装置并检查气密性,关闭d;由e逐滴加入稀硫酸至不再产生气泡为止;③打开d,慢慢鼓入空气10 min;④再称干燥管的总质量为162.4 g。该产品中碳酸钠的质量分数为_______________(结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,下列说法错误的是( )

A.t℃时,将50g a物质加入到50g水中充分搅拌,可得到90g a的饱和溶液
B.a、b、c三种物质均属于易溶物质
C.a中含有少量b,可用冷却a的热饱和溶液的方法提纯a
D.将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋中有丰富的资源,海水晒盐后,分离出食盐的海水称为苦卤水,其中含有丰富的MgCl2。工业上以苦卤水为原料制取金属镁(Mg)的流程如下:
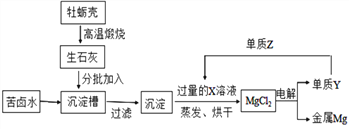
(1)从海水中析出食盐的结晶方法是______________
(2)Y与 Z 反应后的产物溶于水可得 X 溶液,从而实现了 Y 的循环利用,则 Z 的化学式为_____________
(3)烘干后得到的MgCl2中可能含有的杂质是_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D是初中化学常见的四种物质,其中A、B属于相同类别的无机化合物,C、D属于不同类别的纯净物,他们之间有如图所示的转化和反应关系,(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)
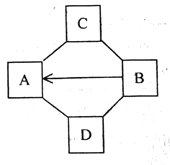
(1)若C是种单质,A-C的化学方程式是__,B→A的基本反应类型是____。
(2)若C是一种非金属氧化物,B-D的化学方程式是____,B→A的化学方程式是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图标示的是有关电水壶的物质组成,请回答以下问题:
(1)写出所标物质中所含金属的元素符号_____.
(2)使用该热水壶烧水,几天后发现热水壶内壁上有水垢,说明使用的水为___水(填“软”或“硬”).
(3)利用厨房的一种常见物质___就可以除去水壶内壁上附着的水垢.
(4)冷开水不能养鱼是因为___.
(5)水和过氧化氢都是由氢、氧两种元素组成的,但其化学性质并不相同,是因为__.

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A~G为初中化学常见的物质。如图所示“→”表示转化关系,“—”表示相互能发生反应。已知A是人体胃液中含有的酸,E是最轻的气体,B和D所含元素相同。请回答:
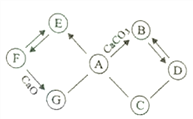
(1)写出下列物质的化学式:A__________,D____________。
(2)G物质的一种用途_________________________。
(3)写出F→E的化学反应方程式_____________________,该反应的基本类型为_______反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
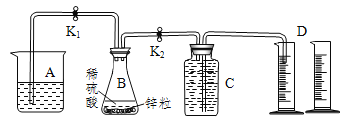
【题目】某化学兴趣小组用如图装置进行“市售锌粒和硫酸反应制取氢气的条件选择”的探究:当B中的化学反应趋于平稳后,每间隔一分钟收集一次氢气。不同条件下,每分钟收集到氢气的体积如下表:
实验 序号 | 硫酸 浓度 | 饱和硫酸 铜溶液体 积/mL | B中反应 达到平稳 的时间/min | 第1分钟 收集氢气 体积/mL | 第2分钟 收集氢气 体积/mL | 第3分钟 收集氢气 体积/mL |
1 | 20% | 0 | 5.4 | 6.1 | 11.9 | 13.7 |
2 | 20% | 0.5 | 2.5 | 23.9 | 32.1 | 33.5 |
3 | 30% | 0.5 | 1.1 | 60.7 | 89.9 | 90.1 |
4 | a% | 3.0 | 0.8 | 55.7 | 66.0 | 61.4 |
(1)关闭K2、打开K1,观察到___________________________,说明B中反应达到平稳,可以开始收集气体。
(2)实验1、2是对比实验,分析上表,说明该对比实验的目的是________。
(3)实验4是探究饱和硫酸铜溶液的体积对实验的影响,a值应为______(填选项)。
A.25 B.30 C.35 D.40
(4)分析上表,市售锌粒和硫酸反应制取氢气的条件应该选择实验________(填实验序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com