

分析 总质量减去滤液得到滤渣也就可以求算去氧化铁的质量,溶液的质量增加量也就是氧化铁的质量.根据氧化铁的质量和对应化学方程式可以求算氯化铁的质量以及消耗的氢氧化钠的质量,和生成的氯化钠的质量,由于涉及多步反应,所以可以用关系式法.
解答 解:
配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量为200g×14.6%÷36.5%=80g;
写出反应①中发生的化学反应方程式:Fe2O3+6HCl═2FeCl3+3H2O;
加入氢氧化钠发生的反应为FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
设生成的氯化铁的质量为x,参加反应的氢氧化钠的质量为y,生成的氯化钠的质量为z,生成的氢氧化铁的质量为a
由于溶液的质量增加是由于氧化铁溶解所致,所以氧化铁的质量为216g-200g=16g,矿石中氧化铁的质量分数为$\frac{16g}{20g}$×100%=80%,盐酸中HCl的质量为29.2g,所以和氧化铁反应是有剩余的.
由上述反应可得如下关系式
Fe2O3~~~2FeCl3~~~~2Fe(OH)3↓
160 325 214
16g x a
$\frac{160}{16g}$=$\frac{325}{x}$=$\frac{214}{a}$
a=21.4g
由于盐酸是过量的,所以根据最终氯元素和钠元素形成氯化钠可得关系式
HCl∽∽∽NaOH∽∽∽NaCl
36.5 40 58.5
29.2g y z
$\frac{36.5}{29.2g}$=$\frac{40}{y}$=$\frac{58.5}{z}$
y=32g
z=46.8g
氯化铁的质量(x)的比例式:$\frac{160}{16g}$=$\frac{325}{x}$;
氢氧化钠的质量为 32g
所得中性滤液b中溶质的质量分数为$\frac{46.8g}{216g+7.4g+32g-21.4g}$×100%=20%
(6)工业上需要制得含杂质为20%的生铁112t,则需上述赤铁矿的质量为m.
根据铁元素守恒可得
Fe2O3∽∽∽2Fe
160 112
80%m 112t×(1-20%)
$\frac{160}{112}$=$\frac{80%m}{112t×(1-20%)}$
m=160t
故答案为:
(1)80g;
(2)Fe2O3+6HCl═2FeCl3+3H2O;
(3)$\frac{160}{16g}$=$\frac{325}{x}$;
(4)32g;
(5)20%;
(6)160t.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:初中化学 来源: 题型:解答题
| 主食 | 米饭、馒头 |
| 副食 | 红烧鱼块、煎鸡蛋、红烧肉、豆腐汤 |
| 饮料 | 牛奶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2017年哈尔滨市政府为了给同学们创造更优越的学习环境,计划给一部分薄弱学校投资盖 薪新的教学楼,增添教学设施.下列说法错误的是( )
2017年哈尔滨市政府为了给同学们创造更优越的学习环境,计划给一部分薄弱学校投资盖 薪新的教学楼,增添教学设施.下列说法错误的是( )| A. | 建筑用的合成纤维绳索属于合成有机高分子材料 | |
| B. | 楼内墙体内的铁合金属于化合物,是金属材料 | |
| C. | 用到的玻璃钢属于复合材料 | |
| D. | 体育馆的设施有些采用太阳能供电非常环保 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
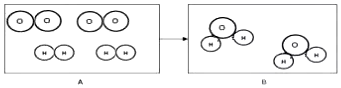
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ①②⑤ | C. | ①④⑤⑥ | D. | ②③⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
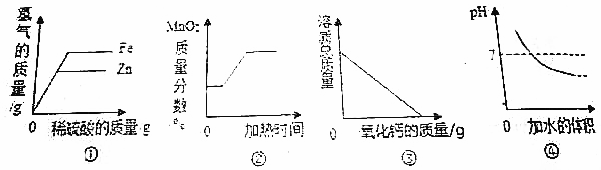
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com