
【题目】食品工业中碘化钾(KI)可用作营养增补剂。碘化钾是白色固体,在空气中久置会“泛黄”变质。某实验小组对碘化钾变质后的成分及变质的条件进行探究。
I.探究变质后的固体成分
(查阅资料)淀粉溶液遇碘(I2)变蓝。
(进行实验)
实验 1
编号 | ① | ② |
操作及现象 | 加热变质后的 KI 固体,黄色消失, 产生的紫色蒸气使淀粉溶液变蓝。 | 向变质后的 KI 固体中滴加稀盐酸, 产生的气体使澄清石灰水变浑浊。 |
II.探究变质的条件
(猜想与假设)常温下,KI 固体“泛黄”变质可能与 O2、CO2 和水蒸气有关。
(进行实验)
实验 2:利用下图装置和表中所列物质分别进行实验,放置相同时间,现象如下表。
装置 | 编号 | ① | ② | ③ | ④ |
| 试管中的物质 | O2 和 H2O | O2 和 CO2 | H2O 和 CO2 | O2、CO2 和H2O |
固体颜色 | 无明显变化 | 无明显变化 | 无明显变化 | 固体泛黄 |
(解释与结论)
(1)实验 1 中石灰水变浑浊的原因是_________(用化学方程式表示)。
(2)由实验 1 中现象推知,“泛黄”变质后的固体中含有的物质是________。
(3)由实验 2 得出“KI 变质一定与 O2 有关”的结论,依据的两个实验是________(填编号)。
(4)由实验 2 推知,KI“泛黄”变质的条件是_________。
III.依据初步结论,深入探究变质的条件
实验 3:分别取相同浓度的 KI 溶液进行实验,在空气中放置相同时间,现象如下表。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
溶液颜色 | 无色 | 浅黄色 | |||
(5)实验 3 中,观察到③~⑤溶液颜色依次加深,推测其原因是________。
(6)由实验 3 推知,KI 固体久置“泛黄”变质过程中,CO2 起到的作用是________。
【答案】CO2+ Ca(OH)2=CaCO3↓ + H2O I2 和 K2CO3 ③和④ O2 、CO2 和 H2O 同时存在 加入酸的量不同 提供酸性环境
【解析】
解:(1)二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)实验1中,产生的紫色蒸气使淀粉溶液变蓝,说明含有碘单质,向变质后的KI固体中滴加稀盐酸,产生的气体使澄清石灰水变浑浊,说明含有碳酸钾;
(3)实验2中,当水、二氧化碳和氧气同时存在时会变黄,只有水和二氧化碳不会变黄,故对比实验③和④能得出“KI变质一定与O2有关”的结论;
(4)由实验2推知,KI“泛黄”变质的条件是与水、二氧化碳和氧气同时存在;
(5)实验3中,观察到③~⑤溶液颜色依次加深,是因为加入的酸的量不同;
(6)二氧化碳的水溶液是酸性的,故此实验中二氧化碳起到的是提供酸性环境的作用。


科目:初中化学 来源: 题型:
【题目】α-丙氨酸是合成蛋白质的基础物质之一,其分子结构如右图所示。下列有关该物质的说法不正确的是
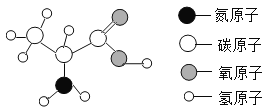
A. 从分类角度看:α-丙氨酸属于有机物
B. 从量的角度看:在α-丙氨酸中碳、氢、氧、氮各元素的原子个数比为3:7:2:1
C. 从变化角度看:α-丙氨酸全燃烧后的产物是二氧化碳和水
D. 从微观角度看:α-丙氨酸是由分子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“化学来源于生活,同时服务于生活”.请运用所学的化学知识,回答下列问题:

(1)“洗衣凝珠”是由一层薄膜包裹洗衣液制成的新型洗涤产品,该薄膜的主要化学成分是可溶于水的聚乙烯醇(简称PVA)塑料,聚乙烯醇的化学式为(C2H4O)n.试回答:
①聚乙烯醇属于_____(填“金属材料”、“有机合成材料”、“硅酸盐材料”、“复合材料”之一).
②醋酸(CH3COOH)是合成PVA的原料之一,醋酸分子中氢原子与碳原子的个数比为_____(填最简整数比).
③在古代,人类就掌握了钻木取火的方法,钻木之所以能取火,是因为①木头具有可燃性;②木头的温度达到了着火点;③_____.
(2)“珍爱生命,远离烟草,拒绝毒品”是一种健康向上的人生理念,尼古丁(C10H14N2)是烟草中含有的剧毒的物质,“冰毒”(C10H15N)是一种毒性强烈的毒品.下列有关说法中,不正确的是_____(填写字母序号).
A 尼古丁和“冰毒”所含元素种类相同 B 尼古丁和“冰毒”性质完全相同
C “冰毒”具有强烈的毒性,千万不可尝试 D 被动吸烟也是对人体健康有害的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
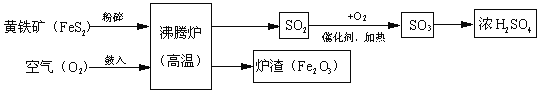
(1)写出流程图中一种氧化物的名称___________。
(2)将黄铁矿粉碎,目的是______________________________________________。
(3)流程中SO2转化为SO3的化学方程式为_________________________________。
(4)实验室稀释浓硫酸应注意什么?_______________________________________________________。
(5)炉渣(Fe2O3)在工业上可用来_____________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
谈到农药,人们可能想到它对人体健康和环境的危害,其实农药在农业生产上起着重要的作用。目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。
实验人员分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
清水浸泡。图 1 呈现出两种农药的去除率随浸泡时间的变化。
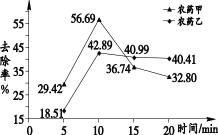
洗洁精清洗。实验选择了 6 种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到 60%以上,最高可达到 84%。
碱性溶液浸泡。食用碱(Na2CO3 和 NaHCO3) 溶液有利于农药分解。图2表示不同浓度的食用碱溶液对农药去除率的影响。
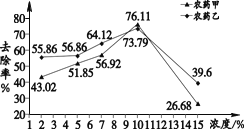
希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。依据文章内容,回答下列问题。
(1)依据图 1 分析,去除农药残留的最佳浸泡时间是________ min。
(2)NaHCO3 的组成元素中,非金属元素有________种。
(3)食用碱溶液的 pH________ 7(填“>”、“=”或“<”)。
(4)用食用碱溶液浸泡含有农药甲的蔬菜时,要想超过清水浸泡的最大去除率,可以选取的浓度是________(填序号,下同)。
A 2% B 8% C 10% D 15%
(5)下列说法正确的是________。
A 采用清水浸泡去除农药的时间不宜过长
B 多数洗洁精对农药的清洗效果比清水浸泡的好
C 食用碱的去除效果较好,是因为在浸泡过程中农药发生了化学变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确定该固体粉末的成分,进行了如下实验:
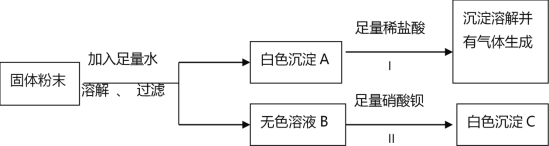
回答下列问题:
(1)反应I的化学方程式为________。
(2)白色沉淀C是______(填化学式)。
(3)原固体粉末中一定不含______(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(学生板演)该反应的化学方程式_____.
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(假设猜想)针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是_____.
(实验探究)
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有_____.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究.
实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | ____ | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的.
(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出实验探究(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是_____.
(2)实验方案中也有一个是错误的,错误的原因是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法正确的是( )
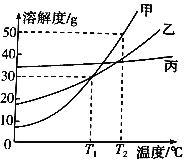
A.T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙
B.T2℃时,将甲、乙的饱和溶液均降温到T1℃时,析出晶体的质量相等
C.若丙中混有少量的甲,可采用降温结晶的方法提纯丙
D.T1℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电动独轮车是新一代的节能、环保、便携的代步工具.它体形小巧、携带方便,最轻的一款只有10Kg,可以直接放进汽车后备箱,提到家里或是办公室.

(1)制造电动独轮车所用的主要材料最好是 ;(在A.B、C中选填)
A.韧性好、硬度大的锰钢
B.强度好、密度小的铝合金
C.抗腐蚀性好的不锈钢
(2)电动独轮车充电2个小时,可以行驶25Km,短途代步非常方便,可以代替公交和地铁.电动独轮车在行走时的全部能量转化是 .
(3)电动独轮车中许多电线为铜制的,铜能和浓硝酸反应,生成二氧化氮、硝酸铜和水,其反应方程式为 ,反应后氮元素的化合价为 .
(4)在环境污染日益严重的背景下,电动独轮车的大力普及,可缓解资源的消耗并减少 、 等空气污染物的排放.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com