
 ④
④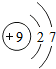 ⑤
⑤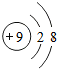
| A. | ①可表示两个氮原子 | B. | ③可表示一种化合物分子 | ||
| C. | ②和⑤均表示阳离子 | D. | ④和⑤表示的微粒化学性质相同 |
分析 A、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
B、由不同种原子构成的分子为化合物的分子,进行分析判断.
C、当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
D、决定元素化学性质的是原子的最外层电子数,进行分析判断.
解答 解:A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N,故选项说法错误.
B、③是由两种原子构成的一种分子,可表示一种化合物分子,故选项说法正确.
C、②Mg2+带2个单位的正电荷,属于阳离子;⑤质子数=9,核外电子数=10,质子数<核外电子数,为阴离子;故选项说法错误.
D、决定元素化学性质的是原子的最外层电子数,④和⑤粒子的最外层电子数不同,化学性质不相似,故选项说法错误.
故选:B.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、粒子结构示意图等)的书写方法是正确解答此类题的关键.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 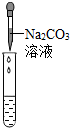 | 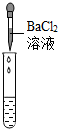 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
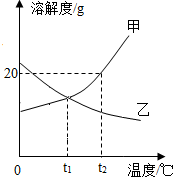 甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )| A. | 升温能使甲物质的不饱和溶液变为饱和溶液 | |
| B. | t2℃时,乙物质的溶解度比甲物质的溶解度大 | |
| C. | t1℃时,甲、乙两种饱和溶液的溶质质量分数相同 | |
| D. | t2℃时将甲、乙两饱和溶液降温到t1℃时,乙析出晶体较多 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质类别不同 | B. | 原子的质子数不同 | ||
| C. | 原子的电子数不同 | D. | 原子的质量不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 丁>丙>甲>乙 | B. | 乙>甲>丙>丁 | C. | 丙>丁>甲>乙 | D. | 丁>丙>乙>甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com