
科目:初中化学 来源: 题型:解答题
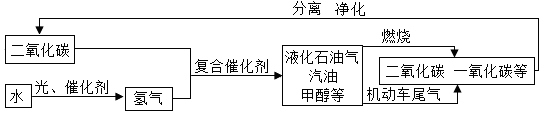
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
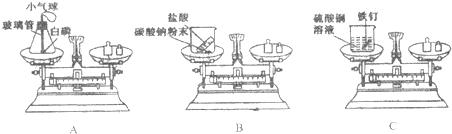
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热蒸发溶剂后,再降至原温度 | B. | 加入一定量的硝酸钾 | ||
| C. | 降温至溶液刚好达到饱和 | D. | 降温后使其析出部分晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 把铝片打磨后,放入装有a:硫酸铜溶液烧杯中,观察 | 铝片表面覆盖一层b:红色的铜 | 三种金属的活动性由强到弱的顺序为: e:铝、铜、银 |
| 把铜片打磨后,放入装有c:硝酸银溶液烧杯中,观察 | 铜片表面覆盖一层d:银白色的银 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
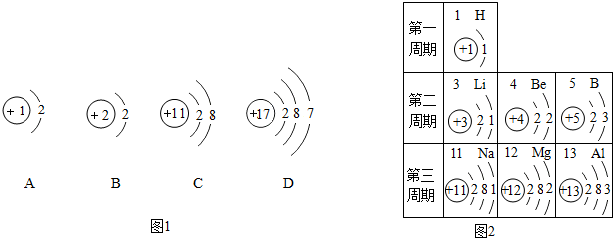
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com