
分析 (1)锌和稀硫酸反应生成硫酸锌和氢气,根据质量守恒定律可以计算生成氢气的质量;
(2)并据溶质的质量分数计算即可.
解答 解:(1)生成氢气的质量为:6.5g+100g-106.3g=0.2g;
(2)设生成硫酸锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
161 2
x 0.2g
$\frac{161}{x}=\frac{2}{0.2g}$
x=16.1g
(2)剩余溶液中溶质的质量分数=$\frac{16.1g}{106.3g}$×100%=15.1%
答:(1)0.2;
(2)剩余溶液中溶质的质量分数为15.1%.
点评 根据质量守恒定律,计算氢气的质量,并掌握方程式计算的解题格式,溶质的质量分数的计算方法.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱溶液洒在衣服上,用水冲洗后再涂上硫酸溶液 | |
| B. | 洒在桌子上的酒精燃烧起来,立即用湿抹布或沙子盖灭 | |
| C. | 浓硫酸洒在皮肤或衣服上,立即用大量水冲洗后再涂上3%~5%的碳酸氢钠溶液 | |
| D. | 进入久未开启的菜窖前先做灯火实验 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
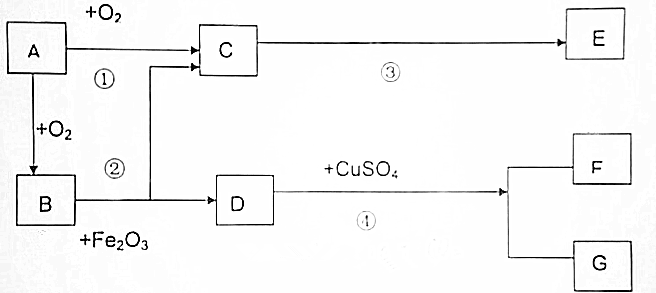
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂试剂 | 除杂方法 | |
| A | H2O | MnO2 | 活性炭 | 吸附、过滤 |
| B | 铁粉 | 铜粉 | 盐酸 | 加入足量盐酸,充分反应后过滤,洗涤,干燥 |
| C | CO2 | CO | O2 | 点燃 |
| D | NaCl | Na2CO3 | 盐酸 | 加入盐酸至不再产生气泡,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用稀盐酸除铁锈:Fe2O3+6HCl→2FeCl2+3H2O | |
| B. | 工业上用氢氧化钠制碳酸钠:Na2CO3+Ca(OH)2→CaCO3↓+2NaOH | |
| C. | 用电解水的方法测定水的组成:2H2O→2H2↑+O2↑ | |
| D. | 用二氧化碳制碳酸饮料:CO2+H2O→H2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com