
【题目】S-诱抗素是一种植物的生长平衡因子,是所有绿色植物均含有的纯天然产物,对光敏感,属强光分解化合物,其化学式为C15H20O4。下列关于S-诱抗素的说法正确的是(____)
A S-诱抗素中氢元素和氧元素的质量比为5:1
B S-诱抗素的相对分子质量为264
C S-诱抗素由39个原子构成
D S-诱抗素中质量分数最大的元素是_____
科目:初中化学 来源: 题型:
【题目】某同学设计了如图A—F气体制取与性质的组合装置。打开活塞K,很快看到F装置中蜡烛由下至上依次熄灭。请根据下图回答问题
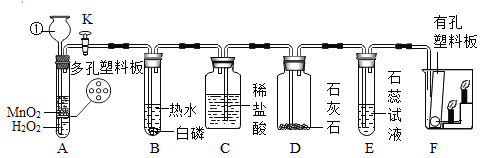
(1)仪器①的名称为:_____
(2)利用A装置制取气体的优点_____;A装置中发生的化学反应方程式为:_____。
(3)E装置中观察到石蕊试液变红,用化学反应方程式解释产生该现象的原因:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验室的废水中含有大量AgNO3、Al( NO3)3和Fe( NO3 )2,课外小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体。实验方案如下:
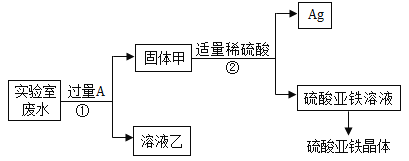
(1)溶液乙中所含的溶质有哪些______________? (用化学式表示)
(2)写出步骤②中发生反应的一个化学方程式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁、M是初中化学常见的化合物,它们之间的关系如图所示(部分物质已经略去)。已知甲、乙、丙、丁是四种不同类别的化合物,M与甲属于同种类别的化合物。
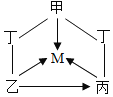
(1)若甲是大理石的主要成分,乙常用作干燥剂,乙转化为丙的化学方程式为___________。
(2)若丙的俗称是纯碱,甲与丁溶液混合可以得到黄色溶液,则甲的化学式为___________;乙转化为M的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列仪器用于实验室里制备气体的实验。分析回答问题:

(1)用分解高锰酸钾的方法制取O2。
①有关反应的化学方程式为__________。
②向试管内装入高锰酸钾之前,必须完成的操作是_________。
③收集满氧气后,将毛玻璃片的_________(选填“光滑”或“磨砂”)面与集气瓶口接触,盖上集气瓶口。
(2)通常状况下,二氧化氮是一种密度比空气大的气体,能与水发生反应;在实验室制取少量二氧化氮的方法:常温下铜和浓硝酸反应,生成硝酸铜、水和二氧化氮。
①组装制取NO2的发生装置,需选择上图中的a、g、j和_________。
②若用下图装置来收集NO2,NO2应从_________端进入集气瓶(选填“A”或“B”)。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾( K2FeO4)是一种新型、高效、多功能水处理剂。制备高铁酸钾的工艺流程如图所示:
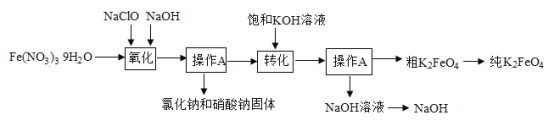
(1)操作A的名称是_____。
(2)制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠溶液中加人饱和KOH溶液,即可析出高铁酸钾。析出高铁酸钾的过程中反应的化学方程式为_____,由此可知,在工序生产控制温度下,高铁酸钠和高铁酸钾两种物质溶解度较大的是_____。
(3)该流程中可循环利用的物质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾和氯化铵的溶解度曲线如图所示,由图甲获得的信息中,不正确的是
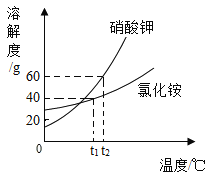
A.两种物质的溶解度均随温度的升高而增大
B.t1℃时,硝酸钾的溶解度大于氯化铵的溶解度
C.t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为2:5
D.t2℃时,硝酸钾饱和溶液比氯化铵饱和溶液的溶质质量分数大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取少量甲烷,可用少量无水醋酸钠(CH3COONa)和碱石灰(NaOH和CaO的固体混合物)的混合物加热来制取,反应的化学方程式为: ![]() 。实验结束后,大家将反应后的固体加入适量水中,经充分溶解、过滤后得到大量滤渣,小明认为这些滤渣中一定含有碳酸钙,还可能含有CaO。经讨论,大家否定了CaO的存在,其理由是_____________(用化学方程式表示)。接着大家对滤液的成分进行探究。
。实验结束后,大家将反应后的固体加入适量水中,经充分溶解、过滤后得到大量滤渣,小明认为这些滤渣中一定含有碳酸钙,还可能含有CaO。经讨论,大家否定了CaO的存在,其理由是_____________(用化学方程式表示)。接着大家对滤液的成分进行探究。
[提出问题]滤液中溶质的成分是什么?经讨论,同学们认为滤液中一定含有NaOH,其原因是_________。他们对滤液中含有的其他溶质进行了猜想:
[猜想与假设]猜想一:Na2CO3;猜 想二:Ca(OH)2
[设计并实验]实验一:取少量滤液于试管中,向试管中滴入几滴无色酚酞溶液,溶液变红色,溶液呈碱性。小明认为该实验没有必要做,你是否同意,并说明理由_____________。
实验二:取少量滤液于试管中,向其中加入过量稀盐酸,观察到____________。证明猜想一不成立。
实验三:取少量滤液于试管中,向试管中滴入适量的碳酸钠溶液,观察到产生白色沉淀,证明猜想_________成立。
[反思应用](1)实验二中 加入“过量”稀盐酸的目的是_________。
(2)甲烷是一种可燃性气体,因此,, 在点燃前要注意安全,应进行的操作是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛和钛合金因具有强度高、耐腐蚀性好、耐热性高等特点而被广泛用于各个领域。以钛铁矿(主要成分为FeTiO3)为原料制备金属钛的工艺流程如图所示:

(1)步骤②中根据TiCl4、FeCl3的_______________不同进行蒸馏分离;
(2)步骤③中氩气不是催化剂,则反应中氩气的作用是_______________;写出该步骤中反应的化学方程式_____________。
(3)整个工艺流程中可以循环使用的物质有____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com