
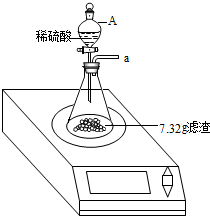
 某兴趣小组对月饼包装盒中的“脱氧剂”很好奇,他们观察“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.
某兴趣小组对月饼包装盒中的“脱氧剂”很好奇,他们观察“脱氧剂”外包装标注的成分为铁粉、活性炭和氯化钠,打开发现灰黑色的固体中还夹杂着少量红棕色粉末.分析 (1)根据氯化钠能溶于水,铁粉、活性炭不易溶于水,可通过加水溶解掉氯化钠进行分析;
(2)样品在稀硫酸中除了Fe、Fe2O3分别能与稀硫酸反应外,还存在反应:Fe+Fe2(SO4)3=3FeSO4.因此,小明用产生H2的质量计算样品中铁的质量不合理;
(3)根据生成的氢气的质量可求出与硫酸反应的铁的质量,可求出铁的质量.
解答 解:(1)将样品加足量水充分搅拌溶解,将样品中的氯化钠溶解掉了;故填:溶解样品中氯化钠,并间接得到氯化钠的质量;
(2)样品在稀硫酸中除了Fe、Fe2O3分别能与稀硫酸反应外,还存在反应:Fe+Fe2(SO4)3=3FeSO4.因此,小明用产生H2的质量计算样品中铁的质量不合理.实际上,样品中单质铁的质量应该是与酸反应消耗的铁和与Fe2(SO4)3反应消耗铁的质量总和.
故填:样品中的铁,除了与稀硫酸反应生成H2外,还有一部分铁与硫酸铁溶液反应;
(3)因为脱氧剂还没有失效.设生成0.1g氢气需要铁的质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.1g
$\frac{56}{x}$=$\frac{2}{0.1g}$
x=2.8g
即样品中铁的质量是2.8g.
由上述计算可知,铁与氧化铁的质量为:7.32g-1.82g-2.8g=2.7g.
设与硫酸铁反应的铁的质量为z
由于Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+Fe2(SO4)3=3FeSO4
可得:Fe~Fe2(SO4)3~Fe2O3
56 160
z $\frac{160z}{56}$
所以:z+$\frac{160z}{56}$=2.7g 解得 z=0.7g
10g该样品中铁粉的质量为:2.8g+0.7g=3.5g
故答案为3.5g.
点评 解答本题的关键是要掌握铁的物理性质和化学性质两方面的知识及其化学方程式的书写方法并结合信息给与的数据,只有这样才能对问题做出正确的判断,难度较大.


科目:初中化学 来源: 题型:填空题
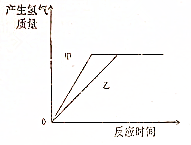 足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.
足量的镁、铁分别与等量的稀硫酸反应,反应的方程式Mg+H2SO4═MgSO4+H2↑、Fe+H2SO4═FeSO4+H2↑,反应速率较快的是镁,则在图中甲表示镁,乙是铁.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食用小苏打作焙制糕点的发酵成分 | |
| B. | 用红墨水、柠檬黄、果绿等将番薯条染色 | |
| C. | 用工业酒精勾兑水来生产低成本白酒 | |
| D. | 使用超量来硝酸钠作为食品保鲜剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 40g | B. | 140g | C. | 136 g | D. | 100 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com