
如图是A、B两种固体物质的溶解度曲线下列说法中错误的是( )

A. t1℃时A、B的溶解度相等
B. t2℃时,A的饱和溶液中溶质的质量分数为 ×100%
×100%
C. A、B的溶解度都随温度升高而增大
D. 将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了
B 【解析】A、由溶解度曲线可知,t1℃时A、B的溶解度相等,该选项说法正确; B、t2℃时,A的饱和溶液中溶质的质量分数为:×100%,该选项说法错误; C、由溶解度曲线可知,t1℃时A、B的溶解度都随温度升高而增大,该选项说法正确; D、将t2℃时B的饱和溶液降温到t1℃时,溶液仍然是饱和溶液,溶解度减小,溶质质量分数也减小,溶液变稀,该选项说法正确. 故选:B....科目:初中化学 来源:江苏省淮安市2018届九年级下学期模拟测试(一)化学试卷 题型:单选题
下列实验操作中正确的是
A.  处理废弃固体药品 B.
处理废弃固体药品 B. 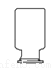 保存二氧化碳气体
保存二氧化碳气体
C.  稀释浓硫酸 D.
稀释浓硫酸 D.  存放稀硫酸
存放稀硫酸
查看答案和解析>>
科目:初中化学 来源:内蒙古赤峰市2018届九年级中考模拟化学试卷 题型:单选题
下列离子能在pH=11的溶液中大量共存的是
A. K+、NO3-、Na+、OH- B. CO32-、K+、Cl-、Ca2+
C. H+、Ba2+、Cl-、SO42- D. K+、OH-、SO42-、Cu2+
A 【解析】试题分析:pH为11的水溶液显碱性,水溶液中含有大量的OH﹣.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可. 【解析】 pH为11的水溶液显碱性,水溶液中含有大量的OH﹣. 【解析】 A、四种离子间不能结合成沉淀、气体或水,能在碱性溶液中大量共存,故选项正确. B、CO32﹣、Ca2+两种离子能结合成碳酸钙沉...查看答案和解析>>
科目:初中化学 来源:四川资阳雁江区2018届九年级初中毕业班适应性检测化学试卷 题型:单选题
下列是几种粒子的结构示意图,有关说法正确的是( )
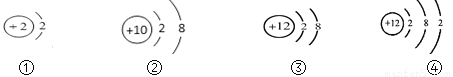
A. ①和④两种粒子的化学性质相似 B. ②和③表示的粒子均为离子
C. ③和④属于同种元素的不同粒子 D. ③表示的粒子的符号为Mg+2
C 【解析】A、元素原子的最外层电子数相同的元素的化学性质相似。但是①只有一个电子层,且是2,属于稳定结构,不易得失电子,③易失去2个电子,所以化学性质不相似,错误;B、②中质子数等于核外电子数,属于原子,错误;C、元素的种类由质子数决定。由图示可知③和④的质子数相同,属同种元素,正确;D、③表示的粒子的符号为Mg2+,错误。故选C。查看答案和解析>>
科目:初中化学 来源:安徽省濉溪县2018届九年级第三次模拟考试化学试卷 题型:科学探究题
某化学兴趣小组通过探究活动学习和理解化学知识。请你一起研究学习,并回答有关问题。

研究问题:水溶液中复分解反应的实质
相关信息:(Ⅰ)电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小。
(Ⅱ)相同温度下同种溶液电导率越大,离子浓度越大。
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示。
①写出Ba(OH)2与H2SO4反应的化学方程式________________________。
②M点时电导率为零,离子浓度也几乎为零,此时混合液体静置后呈______色;
③通过对甲曲线的分析,下列说法错误的是_____(填序号)。
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示。
①通过对乙曲线的分析,下列说法正确的是________(填序号)。
A.实际参加反应的是Ba2+和SO42﹣结合成了BaSO4,Na+和OH﹣还是以离子形式存在于溶液中
B.溶液红色只会变浅,但不会褪去
②N点时,溶液中大量含有的离子是__________________(填离子符号,至少写两种)。
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度_______(填“增大”或“减小”)。
(注意:若答对第(3)小题奖励4分,化学试卷总分不超过60分。)
(3)拓展:①请根据示例仿写离子方程式。示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式:________________________________。
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失。请推测此过程的溶液中Ca2+的浓度变化情况_____________________。
Ba(OH)2+H2SO4=BaSO4↓+2H2O 无 B AB Na+、OH﹣、SO42﹣ 减小 Ba2++SO42﹣=BaSO4↓ 先减小后增大 【解析】本题考查了复分解反应的条件与实质。 (1)①氢氧化钡与硫酸反应生成硫酸钡沉淀和水,反应的化学方程式为Ba(OH)2+H2SO4=BaSO4↓+2H2O; ②甲曲线M点时二者恰好完全反应,溶液呈中性,酚酞为无色,混合液体呈无色...查看答案和解析>>
科目:初中化学 来源:安徽省濉溪县2018届九年级第三次模拟考试化学试卷 题型:单选题
正确的实验操作是实验成功和实验安全的重要保证,下列实验操作正确的是:
A.  点燃酒精灯 B.
点燃酒精灯 B.  液体的量取
液体的量取
C.  取用固体药品 D.
取用固体药品 D.  测定溶液pH
测定溶液pH
查看答案和解析>>
科目:初中化学 来源:2018年福建省永春县化学质检试卷 题型:推断题
A、B、C、D、E是初中化学常见的五种物质,它们分别是单质、酸、碱、盐、氧化物中的一种,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,其相互反应情况如图所示(短线“一”相连的物质间能反应,箭头“→”表示能转化)。
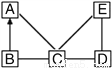
(1)构成A的微粒是_______(填微粒名称); C的水溶液中阳离子符号是______。
(2)D可由两种氧化物反应生成,请写出化学方程式:_________。
(3)写出一个E与D反应可能的化学方程式:_______________。
铁原子 H+ CaO + H2O = Ca(OH)2 Na2CO3 + Ca(OH)2 = CaCO3↓+2NaOH (或K2CO3 + Ca(OH)2 = CaCO3↓+ 2KOH) 【解析】B为红棕色固体,那么B为氧化铁;D常用于改良酸性土壤,那么D为氢氧化钙。C即能与氧化铁反应也能与氢氧化钙反应,那么C是一种酸,可能是稀盐酸;氧化铁能转化A,A是单质,故A可能是铁;E是一种盐,既能与酸...查看答案和解析>>
科目:初中化学 来源:辽宁省丹东市2018届九年级第二次模拟考试化学试卷 题型:实验题
某化学实验小组为了除去混在N2中的O2,将混合气体通过红热的铜丝网后,发现铜丝网变黑。在研究如何除去黑色物质,回收再利用铜丝网的讨论中,制定了下列方案。


 请根据以上方案回答:
请根据以上方案回答:
(1)乙方案的烧杯中发生反应的化学方程式是(其中B物质自行确定)___________。两种方案相比较,从环保的角度来看,甲方案明显的一个不足之处是____________。
(2)若采用甲乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量____(填“<”、“>”、“=”)铜丝网b的质量。
CuO+H2SO4═CuSO4+H2O 没有对尾气进行处理 > 【解析】(1)由于金属铜是不活泼金属,不和稀酸发生反应,但氧化铜可以和稀酸反应,生反应的化学方程式:CuO+H2SO4═CuSO4+H2O;因此可以选择稀盐酸或稀硫酸除去铜丝表面的氧化铜;再就是需要制取一氧化碳,而且一氧化碳是一种有毒的气体,因此必须对尾气进行处理;(2)由于一氧化碳和氧化铜反应时把氧化铜转化成了金属铜,即表面的...查看答案和解析>>
科目:初中化学 来源:河南省邓州市2018届九年级中考第二次模拟考试化学试卷 题型:填空题
金属铝及其合金有广泛的用途
(1)铝是两性金属,请写出氢氧化铝与烧碱溶液反应生成NaAlO2和一种最常见的溶剂的反应方程式;____
(2)工业上通过电解熔融的Al2O3冶炼铝,在负极上生成的物质是________。
Al(OH)3+NaOH=NaAlO2+2H2O 铝(Al) 【解析】(1)由题意可知,氢氧化铝与NaOH溶液反应生成NaAlO2和H2O,反应方程式是:Al(OH)3+NaOH=NaAlO2+2H2O;(2)工业上通过电解Al2O3冶炼铝,铝离子得到电子形成了铝原子,所以在负极上生成的物质是Al。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com