
【题目】某同学设计以下实验探究氧化铜能否作为过氧化氢分解制取氧气的催化剂,以及影响化学反应速率的因素。
实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | 催化剂种类及用量/g | 氧气体积/mL | 收集氧气所用时间/s |
① | 5 | 10 | 20 | 无 | 100 | - |
② | 5 | 10 | 20 | 二氧化锰1g | 100 | 15 |
③ | 5 | 10 | 40 | 二氧化锰1g | 100 | 8 |
④ | 10 | 10 | 20 | 二氧化锰1g | 100 | 5 |
⑤ | 5 | 10 | 20 | 氧化铜1g | 100 | 22 |
(1)通过实验____和____对比,说明过氧化氢分解的速率与温度有关。
(2)通过实验____和____对比,说明过氧化氢分解的速率与浓度有关。
(3)通过实验____和____对比,说明氧化铜粉末能加快过氧化氢分解速率。
(4)想要证明氧化铜是该反应的催化剂,还需要验证其在反应前后____和____没有发生改变。
(5)①写出氧化铜催化过氧化氢分解的文字表达式:__________。
②根据以上实验得出的结论,在下图中画出有、无氧化铜时过氧化氢分解产生氧气的质量与反应时间的关系图____________。
【答案】② ③ ② ④ ① ⑤ 质量 化学性质 ![]()
【解析】
(1)实验②和③温度不同,其他条件相同,通过实验②和③对比,说明过氧化氢分解的速率与温度有关。
(2)实验②和④过氧化氢浓度不同,其他条件相同,通过实验②和④对比,说明过氧化氢分解的速率与浓度有关。
(3)实验⑤有氧化铜,其他条件与实验①相同,通过实验①和⑤对比,说明氧化钢粉末能加快过氧化氢分解速率。
(4)想要证明氧化铜是该反应的催化剂,还需要验证其在反应前后质量和化学性质没有发生改变。
(5)①氧化铜催化过氧化氢分解生成水和氧气,反应的文字表达式为:![]() 。
。
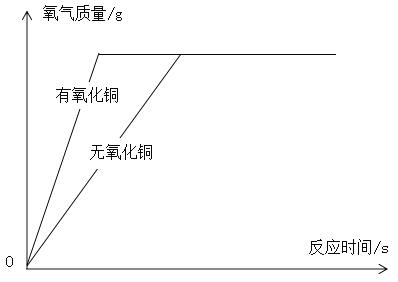
②根据以上实验得出的结论,有、无氧化铜时过氧化氢分解产生氧气的质量一样,但有氧化铜时反应更快,有、无氧化铜时过氧化氢分解产生氧气的质量与反应时间的关系图为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】向一定质量的MgSO4溶液中先后滴加100克Ba(OH)2、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图。下列说法正确的是
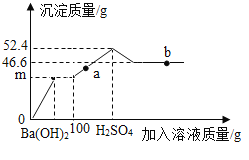
A.a点对应的溶液pH<7
B.b点溶液中的溶质只有1种
C.m=23.3
D.Ba(OH)2溶液溶质质量分数一定等于34.2%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有149.8g氧化铜与稀硫酸反应所得溶液,向其中逐滴加入NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示,请回答问题:
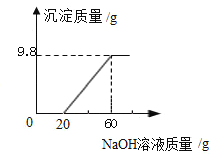
(1)写出产生沉淀的化学方程式____________。
(2)当加入20g氢氧化钠溶液时,溶液中的溶质是____________。
(3)列出根据已知条件求解参加反应的硫酸铜质量(X)的比例式___________。
(4)反应最终所得溶液的溶质质量分数为____________。
(5)若用质量分数50%的氢氧化钠溶液配制实验所需氢氧化钠溶液,需加水质量为___________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】证据推理是科学探究的基本方法。已知某无色溶液A中的溶质是KNO3和Na2CO3。另有一固体样品B,其中可能含有CuSO4和CuO或两者之一。按下图所示进行探究实验,出现的现象如图中所述(设过程中所发生的反应都恰好完全反应)
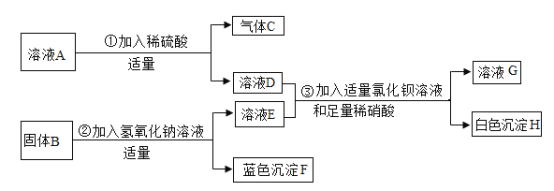
试根据实验过程和发生的现象,填写以下空白:
(1)气体C的化学式为______,将气体C通入紫色石蕊试液,试液变_____色。
(2)蓝色沉淀F的化学式为______
(3)溶液E中大量存在的酸根阴离子是________(填写离子符号)。
(4)固体B中,一定不存在的物质是____(填写化学式),得出此结论的理由是_____。
(5)溶液G中一定大量存在的阳离子有______(填写离子符号)
(6)写出步骤③中发生反应的化学方程式_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年九月,西安市开始实施垃圾分类回收。某街道合金内垃圾桶如图所示,请回答下列问题:

(1)使用铝合金做内筒而不用纯铝的原因是_____(写出一点即可)。
(2)某品牌饮料的空易拉罐应收入_____(填“厨余”、“可回收”或“其他”)筒中。
(3)铁质外筒极易锈蚀,写出一种合适的防锈方法_____;在进行防锈处理之前,要先把铁制品表面的铁锈除掉,写出一种除锈方法_____;铁制品锈蚀的过程,实际上是铁制品跟空气中的_____发生化学反应的过程。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组用下图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。
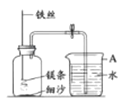
实验前,小组成员提出了不同的猜想。
【猜想与假设】
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,查阅资料知金属镁很活泼,可能会与空气中的氮气反应
【进行实验】
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的2/5 |
【解释与结论】
(1)Mg与氧气反应的化学方程式为_________。
(2)步骤Ⅰ说明装置的气密性_________。
(3)步骤Ⅱ中,关闭止水夹的目的是_________。
(4)推测猜想2成立的现象证据是_________。
【反思与评价】
(5)该小组认为,即使步骤Ⅲ中水的体积恰好占集气瓶体积的1/5,也不能说明猜想1成立,理由是_________。
(6)小组中同学对镁条与瓶中气体的反应提出了进一步的猜想:甲同学认为镁条先与O2反应,乙同学认为镁条先与N2反应。为进一步检验他们的猜想,可以进行的实验操作是:取少量镁条,点燃后迅速放入盛有空气的集气瓶中,待镁条熄灭后,________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下图所示装置验证质量守恒定律。
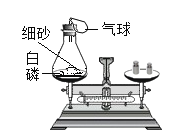
(1)白磷燃烧的化学方程式是_____。
(2)实验过程中,观察到小气球的变化是_____。
(3)实验后冷却至室温再次称量,天平指针_____(填细沙“向左偏”“向右偏”或“不偏转”,下同),若拧松锥形瓶上的胶塞,指针将会_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4,为了测定铁红中铁的质量分数,兴趣小组的同学称取10.0g铁红样品进行如下实验,请你参与过程分析。
(资料)1.草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:![]()
2.浓硫酸具有吸水性,氢氧化钠溶液可以吸收CO2。
3.碱石灰的主要成分是CaO和NaOH,可以吸收水与CO2。
(问题讨论)用下图所示装置实行实验:
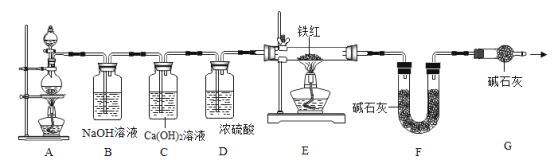
(1)实验前应先_____。
(2)C装置的作用是_____。
(3)对E装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前_____;②停止加热后把反应生成的二氧化碳全部排入F装置中。
(4)写出E装置中所发生反应的一个化学方程式_____。
(数据分析与计算)
(5)充分反应后称得F装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
(6)本实验中如果缺少D装置(不考虑其它因素),则测得样品中铁的质量分数会_____(填“偏小”、“不变”或“偏大”)。
(7)请指出实验装置的一个明显缺陷_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com