

 x=5.3g
x=5.3g y=5.85g
y=5.85g z=4g
z=4g p=11.7g
p=11.7g ×100%=14.3%.
×100%=14.3%.

科目:初中化学 来源: 题型:
| 金属 | Cr | Al | Cu |
| 与盐酸反应发生现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无气泡产生,金属无变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:
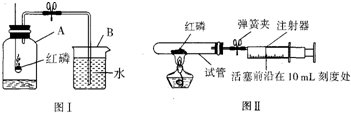
| 点燃 |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| 1 |
| 5 |
| 1 |
| 5 |
| 点燃 |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
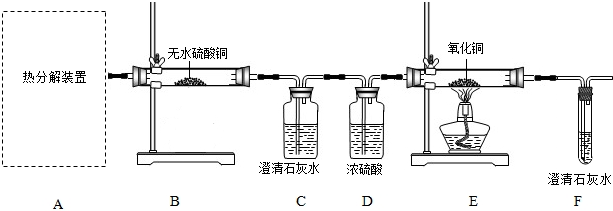
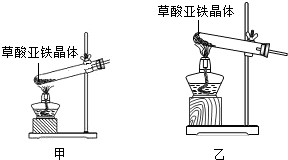
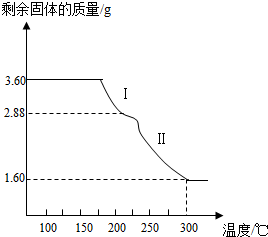
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com