
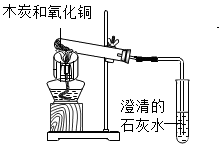
 木炭还原氧化铜的实验装置如图所示
木炭还原氧化铜的实验装置如图所示分析 (1)根据碳和氧化铜在高温条件下反应能生成铜和二氧化碳写出反应的化学方程式;
(2)根据碳具有还原性分析回答;
(3)依据酒精灯火焰加上网罩后火焰集中分析解决;
(4)依据碳还原氧化铜的注意事项分析回答.
解答 解:(1)在高温条件下,碳和氧化铜反应能生成铜和二氧化碳,其方程式为:C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(2)反应完成后,把被加热的试管里的粉末倒在纸上可以看到有亮红色的铜,这是由于碳具有还原性,在高温条件下将氧化铜还原为铜.
(3)酒精灯火焰加上网罩后火焰会集中,从而提高了火焰的温度;(4)试管①中发生的化学反应是碳和氧化铜生成二氧化碳和铜,所以①中的现象应该是固体由黑色逐渐变红;
(4)实验结束时,应先撤出导管,防止停止加热时,试管内温度降低,压强减小,液体进入试管引起试管的炸裂.
故答案为:(1)C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(2)碳具有还原性,在高温条件下将氧化铜还原为铜;
(3)集中火焰提高温度;
(4)撤出导管.
点评 本题考查了常见物质的性质以及有关反应方程式的书写,完成此题,可以依据已有的知识进行,书写方程式时要注意配平.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:初中化学 来源: 题型:选择题
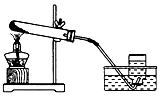
| A. | 试管中盛放的试剂是二氧化锰和双氧水 | |
| B. | 当水槽中导管口一有气泡逸出时,就立即收集O2 | |
| C. | 实验结束时先从水槽中取出导管,再撤走酒精灯 | |
| D. | 实验室还可用向下排空气法收集O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | A、B与酸反应产生氢气质量相等 | |
| B. | D和B(NO3)2溶液中发生了反应 | |
| C. | 四种金属的活动性顺序为A>B>D>C | |
| D. | A、B与盐酸反应中消耗的盐酸质量相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定含有Fe | B. | 滤渣中一定含有Ag | ||
| C. | 滤液中一定含有Al3+、Ag+ | D. | 滤液中一定含有Fe2+、Ag+ |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 取滤渣滴加稀硫酸,可能有气泡产生 | |
| B. | 取反应后的滤液观察,滤液一定呈蓝色 | |
| C. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| D. | 滤液中的溶质最多有两种,滤渣中的物质至少有两种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com