
分析 地壳中含量最多的元素是氧元素.
空气中含量最多的气体是氮气,写出其化学式即可.
最常用的溶剂是水,写出其化学式即可.
地壳中含量最多的金属元素是铝元素,形成的氧化物是氧化铝,写出其化学式即可.
解答 解:地壳中含量最多的元素是氧元素,其元素符号为:O.
空气中含量最多的气体是氮气,其化学式为:N2.
最常用的溶剂是水,其化学式为:H2O.
地壳中含量最多的金属元素是铝元素,形成的氧化物是氧化铝,氧化铝中铝元素显+3价,氧元素显-2价,其化学式为:Al2O3.
故答案为:O;N2;H2O;Al2O3.
点评 本题难度不大,掌握常见化学用语(元素符号、化学式等)的书写方法是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题
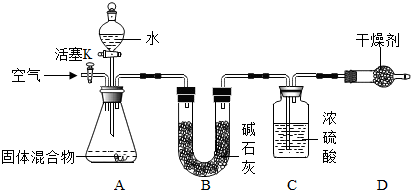
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
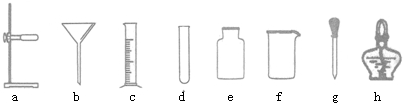
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 常见的混合物:空气、冰水混合物 | B. | 常见的碱:纯碱、熟石灰 | ||
| C. | 常见的氧化物:水、生石灰 | D. | 常见的易燃物:汽油、浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
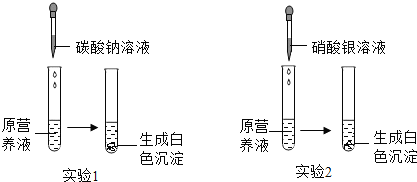
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧时产生大量白烟 | B. | 硫在空气中燃烧,产生淡蓝色火焰 | ||
| C. | 木炭在氧气中燃烧发出明亮白光 | D. | 铁丝在氧气中燃烧生成四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 取少量样品于试管中,加入一定量水,样品全溶解后,滴加足量的稀盐酸(稀硫酸)(填一种溶液名称) | 有气泡产生 | 氢氧化钠已变质 |
| 实验操作 | 实验现象 | 结论 |
| ①取少量样品于试管中,加入一定量水后,样品全溶解后,滴加过量的CaCl2溶液 | 产生白色沉淀 | 氢氧化钠固体部分 变质 |
| ②静置后取上层清液于试管中,滴入2滴酚酞试液 | 溶液变红 |
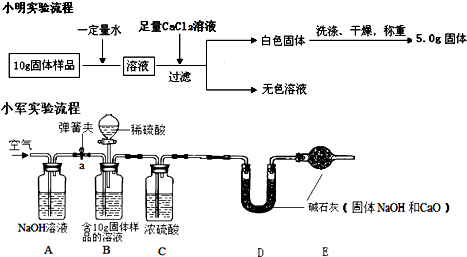
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com