
分析 根据反应的铁的质量和对应的化学方程式求算生成的氢气和氯化亚铁的质量以及消耗的HCl的质量,进而求算对应的质量分数.
解答 解:设5.6g铁完全反应消耗的HCl的质量为x,生成的氢气的质量为y,生成的氯化亚铁的质量为z
Fe+2HCl=FeCl2+H2↑
56 73 127 2
5.6g x z y
$\frac{56}{5.6g}$=$\frac{73}{x}$=$\frac{127}{z}$=$\frac{2}{y}$
x=7.3g
y=0.2g
z=12.7g
该盐酸的质量分数为$\frac{7.3g}{100g}$×100%=7.3%
反应后所得氯化亚铁溶液的质量分数为$\frac{12.7g}{5.6g+100g-0.2g}$×100%≈12.0%
答:
(1)生成0.2克氢气;
(2)该盐酸的质量分数是7.3%
(3)反应后所得氯化亚铁溶液的质量分数是12.0%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:初中化学 来源: 题型:实验探究题
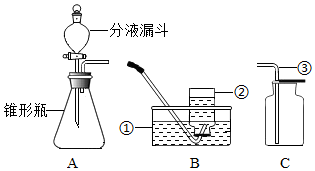
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
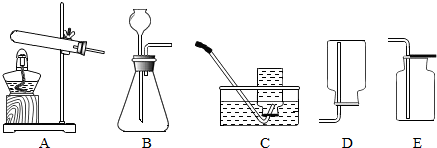
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验次序 | 1 | 2 | 3 | 4 |
| 稀盐酸的质量/克 | 50 | 50 | 50 | 50 |
| 加入样品的质量/克 | 5 | 10 | 15 | 20 |
| 生成CO2的质量/克 | 1.76 | 3.52 | 4.4 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生石灰、熟石灰、烧碱 | B. | 氧化钠、生石灰、干冰 | ||
| C. | 硫酸铝、碳酸钙、石灰水 | D. | 氯气、钡、磷酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸碱指示剂 | B. | AgNO3 | C. | 碘酒 | D. | 酒精 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 实验序号 | 1 | 2 | 3 | 4 |
| 生铁样品的质量/g | 3.0 | 6.0 | 10.0 | 11.0 |
| 生成H2的体积(标准状况下)/L | 1.12 | 2.24 | 3.36 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com