
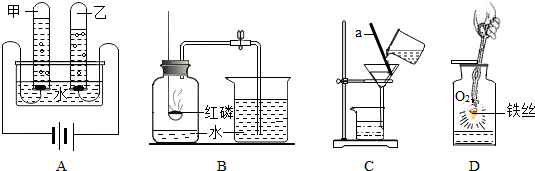
分析 (1)根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住;
(2)进入集气瓶中的水不到五分之一,可从①红磷不足量;②装置的这气密性不好③装置未冷却到室温便打开止水夹来分析;
(3)根据实验室常用仪器解答;根据玻璃棒的作用解答;
(4)根据铁丝燃烧实验的注意事项和现象进行分析;
(5)根据溶液稀释前后溶质质量不变计算;
(6)利用题目所给的数据,结合溶解度的概念解决.
解答 解:(1)由正氧负氢,氢二氧一,可推出乙中产生的是氢气,氢气能够燃烧,产生淡蓝色火焰;
(2)实验完毕,若进入集气瓶中水的体积不到集气瓶中原空气总体积的五分之一,导致这一结果的原因可能是:红磷量不足、装置气密性不好、未冷却到室温就打开止水夹、红磷中含有能燃烧生成其他气体的杂质;
(3)根据实验室常用仪器可知:图中a的名称是玻璃棒;在操作中,它的作用是引流;过滤知识除去不溶性杂质;取少量过滤后得到的水于试管中,加入少量肥皂水,产生的现象是泡沫较少;
(4)实验中集气瓶内放少量水的目的是防止溅落的溶化物炸裂瓶底.铁丝与氧气反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,符合多变一,属于化合反应;
(5)(设需要12%的氯化钠溶液的质量为x,则50g×6%=12%x,x=25g;12%的氯化钠溶液的密度为1.09g/cm3,则所需溶液的体积为25g÷1.09g/cm3≈22.9cm3=22.9mL;需要水的质量为50g-25g=25g(合25mL);
(4)设20℃时氯化钠的溶解度是z,
$\frac{68g-50g}{50g}=\frac{z}{100g}$
z=36g.
答案:
(1)氢气;淡蓝色;
(2)装置漏气(或红磷量不足或未冷却就打开弹簧夹);
(3)玻璃棒;引流;泡沫较少;
(4)防止溅落的溶化物炸裂瓶底;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合反应;
(5)22.9;25;
(6)36
点评 此题难度不大,掌握常见实验的现象、注意事项等是顺利解题的关键所在.有关溶液的基本计算,以及溶解度的有关计算,把计算与实际生产相结合,体现化学的学以致用.


科目:初中化学 来源: 题型:选择题
| A. | 反应前后混合气体中氮气的质量分数不变 | |
| B. | 反应后气体混合物的组成有3种情况 | |
| C. | 若反应后气体是3种气体的混合物,则其中C、O元素的质量比一定小于12:16 | |
| D. | 若反应后气体中有氧气,则容器中C、O元素的质量比大于12:32 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人类的生活和生产都离不开金属材料.
人类的生活和生产都离不开金属材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com