
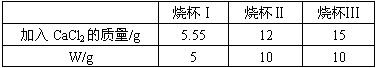
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入CaCl2的质量/g | 5.55 | 12 | 15 |
| W/g | 5 | 10 | 10 |
| 106 |
| 100 |
| Z |
| 10克 |
| 111 |
| 100 |
| X |
| 10克 |
| 100 |
| 117 |
| 10克 |
| Y |
| 10.6克 |
| 11克 |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:广东省模拟题 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:
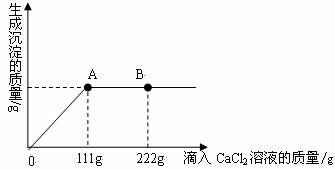
学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,在一烧杯中加入11g样品,加足量水溶解,制成溶液。向其中逐渐滴加溶质质量分数为10%的CaCl2溶液,生成沉淀的总质量与所滴入CaCl2溶液的质量关系曲线如图所示。请根据题意回答问题:
(1)当滴加了111gCaCl2溶液时,生成沉淀的总质量为 g。
(2)当滴加CaCl2溶液至图中B点时,烧杯中溶液里的溶质是(写化学式) 。
(3)样品中Na2CO3的质量分数是多少?(计算结果精确到0.1%)。
当滴加了111gCaCl2溶液时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。
查看答案和解析>>
科目:初中化学 来源:2010年广东省广州市中考化学模拟试卷(一)(解析版) 题型:解答题
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入CaCl2的质量/g | 5.55 | 12 | 15 |
| W/g | 5 | 10 | 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com