
| A. | 水是由氢、氧两种元素组成的 | B. | 水是由氧气和氢气组成的 | ||
| C. | 水通电发生的变化是物理变化 | D. | 水通电发生的反应是化合反应 |
分析 电解水时,与电源负极相连的试管内的气体体积多,与电源正极相连的试管内产生的气体体积少,两者的体积之比大约是2:1;据此结合电解水的实验结论(正氧负氢、氢二氧一),进行分析解答.
解答 解:A、电解水得到氢气和氧气,氢气、氧气分别是由氢元素、氧元素组成的,则说明了水由氢元素、氧元素组成的,故选项说法正确.
B、水是由氢元素和氧元素组成的,不含氢气和氧气,故选项说法错误.
C、水通电分解生成氢气和氧气,有新物质生成,属于化学变化,故选项说法错误.
D、水通电分解生成氢气和氧气,该反应符合“一变多”的特征,属于分解反应,故选项说法错误.
故选:A.
点评 本题难度不大,掌握电解水的实验现象、结论(正氧负氢、氢二氧一)等是正确解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4、Na2O、KCl、CO | B. | Mg(OH)2、CuSO4、HCl、CO2 | ||
| C. | KOH、HNO3、NaCl、SO3 | D. | HCl、NaOH、NaCl、P2O5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C2H5OH和NaCl 溶液(闻气味) | B. | NaOH溶液和稀H2SO4溶液(酚酞试液) | ||
| C. | Ca(OH)2溶液和NaOH溶液(稀盐酸) | D. | KMnO4 和KClO3 (观察颜色) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 一氧化碳 | D. | 二氧化氮 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 李明同学将浑浊的溪水样品倒入烧杯中,先加入明矾粉末来搅拌溶解,静置一会儿后,然后采用右图过滤装置来除去水中难溶性杂质.试回答:
李明同学将浑浊的溪水样品倒入烧杯中,先加入明矾粉末来搅拌溶解,静置一会儿后,然后采用右图过滤装置来除去水中难溶性杂质.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
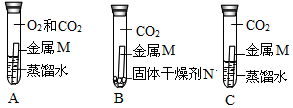
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子核内质子数等于中子数 | B. | 原子核都由质子和中子构成 | ||
| C. | 原子只由质子和电子构成 | D. | 原子中质子数等于核外电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com