
| ���� ���� | �����ԣ�100Ϊ���� | �ܶȣ�g/cm3�� | �۵㣨�棩 | Ӳ�ȣ�10Ϊ���� |
| A | 99 | 8.92 | 1083 | 3 |
| B | 61 | 2.70 | 660 | 2.9 |
| C | 17 | 7.86 | 1535 | 5 |
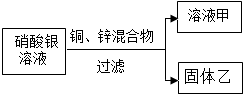
���� ��1��������������������Ԫ����ɵĴ��������һ������Ԫ�ؽ��з�����
��2�����ݽ������Ͻ���������ʷ������
��3�����ݷ�Ӧԭ��д����Ӧ�Ļ�ѧ����ʽ���
��4��һ����̼���������ڸ����·�Ӧ�������Ͷ�����̼��д����Ӧ�Ļ�ѧ����ʽ���ɣ�
��5���ڽ������˳���У�����ǰ��Ľ�������λ��������Ľ�����������Һ���û��������ɼ��Ϊ��ǰ�ú��ο��ܡ���
��� �⣺
��1����������������Ԫ����ɵĴ��������һ������Ԫ�أ������������������������������������������������ѡ��AD��
��2���ٸ�ѹ����߲��ý���A��ѡ�ý���B����Ҫԭ���ǽ���B�ĵ��ԽϺá��ܶ�С���ڽ����ƳɺϽ��Ӳ�Ȼ�����
��3��Ni��CuSO4��Һ�����û���Ӧ�ķ���ʽΪ��Ni+CuSO4�TCu+NiSO4��
��4��һ����̼���������ڸ����·�Ӧ�������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��5���ڽ����˳����У������Ļ��˳����п��ͭ��������һ����AgNO3��Һ�м���ͭ��п�Ļ�Ϸ�ĩʱ��п������������Ӧ����п��Ӧ���ͭ������������Ӧ��
�������к���п��ͭ�������ֹ��壬˵������Һ��û��������������ͭ����ʱ��������м���ϡ���ᣬп���뷢����Ӧ����ѧ����ʽΪ��Zn+2HCl�TZnCl2+H2����
������Һ������ɫ��˵����ͭ������������Ӧ����������ͭ����ѧ��Ӧ����ʽΪ��Cu+2AgNO3�T2Ag+Cu��NO3��2����ʱ��������һ�����е�����������
�𰸣�
��1��AD��
��2���ٵ����ԽϺá��ܶȽ�С�� �ڣ���
��3��Ni+CuSO4�TCu+NiSO4��
��4��Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��5����Zn+2HCl=ZnCl2+H2���� ��Cu+2AgNO3=Cu��NO3��2+2Ag������
���� ������Ҫ�����˽����йص����ʺͽ������˳���Ӧ�ã��ѶȲ�����Ҫ��ǿ���䣮


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
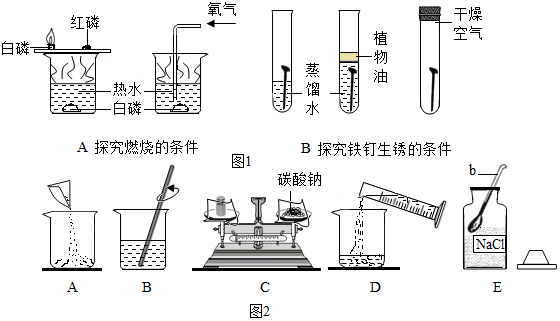
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͭ | B�� | ϡ���� | C�� | �������� | D�� | ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
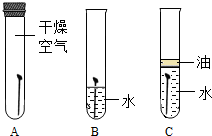
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 KNO3��KCl�ڲ�ͬ�¶�ʱ���ܽ�������ʾ����ش��������⣺
KNO3��KCl�ڲ�ͬ�¶�ʱ���ܽ�������ʾ����ش��������⣺| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| �ܽ�� | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 95.5 | 110 | 138 |
| KC1 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com