
【题目】根据下列反应事实写出相应的化学方程式。
(1)过氧化氢溶液和二氧化锰混合制氧气:_____。
(2)铜和硝酸银溶液反应:_____。
(3)在高温下一氧化碳还原氧化铁:_____。
(4)酒精(C2H6O)完全燃烧:_____。
(5)硫酸与氨水中和生成硫酸铵和水:_____。
【答案】2H2O2![]() 2H2O+O2↑ Cu+2AgNO3=Cu(NO3)2+2Ag 3CO+Fe2O3
2H2O+O2↑ Cu+2AgNO3=Cu(NO3)2+2Ag 3CO+Fe2O3![]() 2Fe+3CO2 C2H6O+3O2
2Fe+3CO2 C2H6O+3O2![]() 2CO2+3H2O 2NH3·H2O+H2SO4=(NH4)2SO4+2H2O
2CO2+3H2O 2NH3·H2O+H2SO4=(NH4)2SO4+2H2O
【解析】
(1)过氧化氢溶液和二氧化锰混合制氧气: 2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(2)铜和硝酸银溶液反应: Cu+2AgNO3=Cu(NO3)2+2Ag。
(3)在高温下一氧化碳还原氧化铁: 3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。
(4)酒精(C2H6O)完全燃烧: C2H6O+3O2![]() 2CO2+3H2O。
2CO2+3H2O。
(5)硫酸与氨水中和生成硫酸铵和水: 2NH3·H2O+H2SO4=(NH4)2SO4+2H2O。


科目:初中化学 来源: 题型:
【题目】(3分)下图是某种汽车尾气处理装置中发生化学反应的微观示意图:
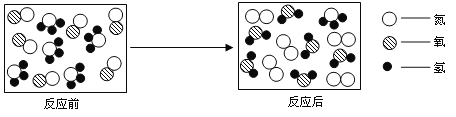
请回答下列问题:
⑴画出氮原子的结构示意图 ,标出氨分子中氮原子的化合价 。
⑵水分子中氧元素的质量百分含量为 。(保留一位小数)
⑶写出装置中发生反应的化学方程式 。
⑷简述汽车尾气中氮的氧化物形成的原因 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢气作为新能源有很多优点,制取与储存氢气是氢能源利用领域的研究热点。
Ⅰ.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制气,其反应可表示为:6ZnFe2O4![]() 6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O
6ZnO+4Fe3O4+O2↑;3ZnO+2Fe3O4+H2O![]() 3ZnFe2O4+H2↑
3ZnFe2O4+H2↑
(1)ZnFe2O4中Fe的化合价为_____。
(2)该循环制氢中不断消耗的物质是_____(填化学式),得到H2和O2的质量比为_____。
Ⅱ.贮氢:合金Mg2Cu是一种潜在的贮氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。该合金在一定条件下完全吸氢生成氢化物和另一种合金,其化学方程式为:2Mg2Cu+3H2![]() 3MgH2+MgCu2。
3MgH2+MgCu2。
(1)熔炼制备Mg2Cu合金时,通入氩气的目的是_____。
(2)氢化物MgH2与水反应生成一种碱,并释放出H2。其化学反应方程式为_____。
(3)11.2gMg2Cu完全吸氢后所得混合物与过量盐酸反应,放出H2的质量为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我省是大豆的主产区,如图是倒伏的大豆。试回答下列问题:

(1)从大豆能做豆腐的角度来看,大豆中含有丰富的营养素是_______________,在酶的作用下,它在人体中和水反应,生成_____________。
(2)为防止大豆倒伏,应施加________肥(填化肥种类,以下相同),为增加其抗旱和抗寒能力应施加___________肥。大豆在生长时,发现叶子边缘枯黄(如图),可施加________肥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铼高温合金材料用于制造航空发动机。在元素周期表中铼元素的某些信息如图所示。下列有关铼的说法错误的是

A. 原子序数为 75B. 属于金属元素
C. 原子核内中子数为 75D. 相对原子质量为 186.2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】南昌大学研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖。请回答下列问题:
(1)右图是镓在元素周期表中的信息以及原子结构示意图。
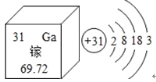
镓的相对原子质量为 ;下列原子结构示意图所对应的元素与镓元素的化学性质相似的是 (填序号);
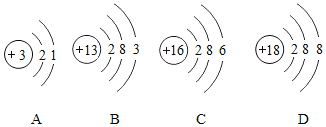
(2)氮化镓(GaN)中镓元素的化合价为+3价,则氮元素的化合价为 价;
(3)传统制备氮化镓的化学原理是:GaCl3+NH3![]() GaN+3X ,其中X的化学式为 。
GaN+3X ,其中X的化学式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家发现,中草药成分中提取的“汉防己碱”能有效避免病毒进入细胞,有助于预防埃博拉感染,其分子式为C38H42N2O6.请回答:
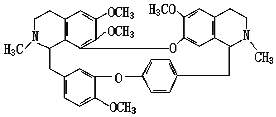
(1)汉防己碱属于_____(填“无机物”或“有机物”);
(2)汉防己碱由_____种元素组成,1244gC38H42N2O6中含氮_____g;
(3)汉防己碱中碳元素与氧元素的质量比是_____(化成最简比)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式碳酸盐广泛应用于工农业生产。
(查阅资料)①碱式碳酸铜可以表示为Cu(OH)2·mCuCO3,是常见的碱式碳酸盐。
②碱式碳酸盐M(OH)2·MCO3不溶于水,与碱式碳酸铜具有相似的化学性质。
③无水硫酸铜是白色粉末,能与水作用生成蓝色固体。
(1)研究小组欲确定某碱式碳酸盐样品M(OH)2·MCO3中金属M的相对原子质量。
(实验装置)
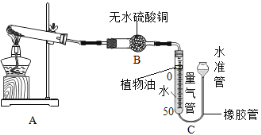
(实验步骤)
①连接装置并检査装置气密性;②准确称量样品的质量;③装药品,调节量气装置两边液面相平,读数;④点燃酒精灯,加热样品至质量不再减少;③冷却到室温;⑥调节量气装置两边液面相平,读数、列式计算。
I.步骤①中检査装置气密性的方法是_____________。
Ⅱ.装置B的作用是________,装置C中植物油的作用是____。
Ⅲ.步骤⑥中调节液面相平的操作是将水准管_____(填“缓慢上移”或“缓慢下移”)。
Ⅳ.若其它操作均正确,仅因下列因素可使M相对原子质量的测定结果偏大的是_____(填序号)。
a.反应前量气管水面在0刻度处,反应后仰视读数 b.样品未分解完全即停止实验
c.量气管中未加植物油
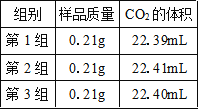
(2)某研究小组仍使用上述装置測定m的值,测得3组数据如表所示。实验测得CO2的体积为__________mL,又已知常温常压下CO2的密度为1.964g/L,据此计算m的值为______(结果保留两位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,下列说法不正确的是( )
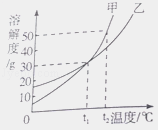
A.t1℃时,甲和乙的溶解度相等
B.甲和乙的溶解度都随温度的升高而增大
C.t1℃时,甲和乙各30g分别加入90g水中,均能完全溶解
D.t2℃时,在100g水中放入60g甲,形成饱和溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com