C
分析:假定物质是纯净物质,分别计算出10克物质与盐酸生成二氧化碳的气体的质量,如一个质量大于4.3克,另一个质量小于4.3克,则就符合条件.
解答:设碳酸盐的化学式为A,相对分子质量是M.
A~CO
2↑
M 44
10克 4.3克
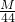
═
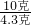
得:M=102.3
∴当碳酸盐的相对分子质量大于102.3,则生成二氧化碳气体的质量就会小于4.3克;当碳酸盐的相对分子质量小于102.3,则生成二氧化碳气体的质量就会大于4.3克.
A、碳酸钙的相对分子质量是100<102.3,碳酸钾的相对分子质量是138>102.3,可以含有碳酸钾.
B、碳酸钙的相对分子质量是100<102.3,氢氧化钠和盐酸不会产生气体,可以含有氢氧化钠.
C、碳酸钙的相对分子质量是100<102.3,碳酸镁的相对分子质量是84<102.3,所以不能呢个含有碳酸镁.
D、碳酸钙的相对分子质量是100<102.3,碳酸钠的相对分子质量是106>102.3,可以含有碳酸钠.
故选C.
点评:掌握这种判断物质组成的方法,记住:如一个质量大于4.3克,另一个质量小于4.3克,则就符合条件.

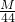 ═
═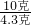


 名校课堂系列答案
名校课堂系列答案