
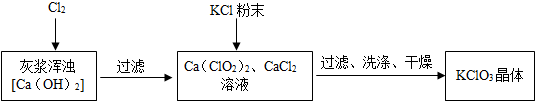
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
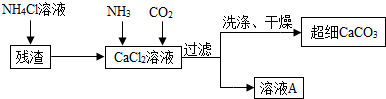
分析 (1)根据氢氧化钙露置在空气中,会与空气中的二氧化碳反应生成碳酸钙进行解答;
(2)找出反应物和生成物,正确书写化学方程式;
(3)根据表格以及复分解反应的定义进行解答;
(4)根据洗涤时既要洗净又不可引入杂质进行解答;
(5)由流程图找出反应物和生成物,正确书写化学方程式,分析循环的物质.
解答 解:(1)因为电石与水反应生成氢氧化钙,其露置在空气中,会与空气中的二氧化碳反应生成碳酸钙,故残渣中主要成分是Ca(OH)2和CaCO3;
(2)由题意可知反应物为氯气和氢氧化钙,反应物为Ca(ClO3)2、CaCl2和H2O,反应的化学方程式为:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O;
(3)由表以及复分解反应的定义,两种化合物相互交换成分可知,KCl与Ca(ClO3)2发生了复分解反应,由于KClO3在常温下溶解度较小,故可结晶析出,得到其固体;
(4)B和C都可以洗涤氯酸钾晶体,但A不可,因为它会引入新的杂质.
(5)由流程图可以看出,反应物为氨气和二氧化碳和氯化钙和水,生成物为碳酸钙和氯化铵,其反应的化学方程式为:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl;因此A溶液的化学式为:NH4Cl;
故答案为:(1)CaCO3;(2)6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O;(3)Ca(ClO3)2;相同温度下,氯酸钾的溶解度小;(4)BC;(5)NH4Cl.
点评 本题属于信息题的考查,综合考察了产物的判断、化学方程式的书写,锻炼了学生的逻辑思维和分析解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 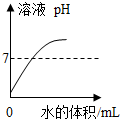 是浓盐酸敞口放置较长时间 是浓盐酸敞口放置较长时间 | |
| B. | 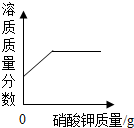 是向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 是向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| C. | 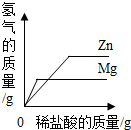 是等质量的Zn和Mg分别与等质量、等质量分数的足量的稀盐酸反应 是等质量的Zn和Mg分别与等质量、等质量分数的足量的稀盐酸反应 | |
| D. | 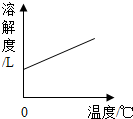 是氢氧化钙的溶解度受温度变化的曲线图 是氢氧化钙的溶解度受温度变化的曲线图 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
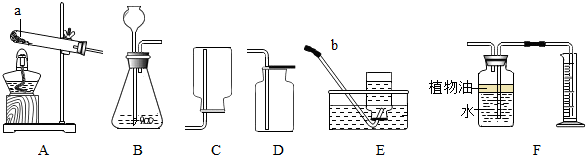
 A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.
A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/kJ | |
| 甲烷 | 2.75 | 56 |
| 碳 | 3.67 | 32 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐 | |
| B. | 用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳 | |
| C. | 经点燃,产生蓝色火焰的气体一定是一氧化碳 | |
| D. | 某溶液中加入稀盐酸无任何明显现象,再加入氧化钡溶液,出现白色沉淀,则原来溶液中一定含有硫酸根离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com