
ÖŲŅŖÖŖŹ¶ĢįŹ¾
1”¢¼ī£«ŃĪ”¢ŃĪ£«ŃĪ·“Ó¦µÄ·“Ó¦ĪļÓ¦ČÜÓŚĖ®£¬Éś³ÉĪļÖŠŅ»°ćŅŖÓŠ³Įµķ
2”¢¼ģijČÜŅŗÖŠŹĒ·ńŗ¬ÓŠCO32—”¢SO42—”¢Cl—µÄĖ³ŠņĪŖ£ŗȔѳʷ¼ÓČė¹żĮæµÄĻ”ĻõĖį
£ØÓŠĘųÅŻĖµĆ÷ÓŠĢ¼Ėįøł”¢¹żĮæÄæµÄŹĒ³ż¾”Ģ¼ĖįøłĄė×Ó£©£¬Č»ŗóŌŁ¼ÓČė¹żĮæĻõĖį±µ£ØČēÓŠ³ĮµķĖµĆ÷ÓŠĮņĖįøł”£¹żĮæĪŖ³ż¾”ĮņĖįøłĄė×Ó£©£¬×īŗó¼ÓČėĻõĖįŅų£ØČē³öĻÖ³ĮµķĖµĆ÷µÄĀČĄė×Ó£©
3”¢ĘųĢåĪüŹÕ£ŗ
NaOH¹ĢĢå£ŗĪüĖ®ŗĶĖįŠŌĘųĢå£ØČēÉŁĮæµÄ¶žŃõ»ÆĢ¼£¬¶žŃõ»ÆĮņ”¢ĀČ»ÆĒā”¢Įņ»ÆĒā£©
NaOHČÜŅŗ£ŗĪüĖįŠŌĘųĢå£ŗCO2”¢SO2”¢HClµČ
ÅØĮņĖį£ŗĖ®ŗĶ¼īŠŌĘųĢå£ŗNH3
4”¢ÓĆÅØŃĪĖįÓė“óĄķŹÆ·“Ó¦ÖĘČ”¶žŃõ»ÆĢ¼Ź±£¬Éś³ÉĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®£¬²»±ä»ė×Ē£¬ŌŅņŹĒ»ģÓŠĀČ»ÆĒā
5”¢ÓĆÅØŃĪĖįÓė“óĄķŹÆ·“Ó¦ÖĘČ”¶žŃõ»ÆĢ¼Ź±£¬Éś³ÉĘųĢåĶØČė×ĻÉ«ŹÆČļČÜŅŗ£¬ŹÆČļČÜŅŗ±äŗģµÄŌŅņæÉÄÜŹĒCO2ÓėĖ®·“Ӧɜ³ÉĮĖH2CO3£¬Ņ²æÉÄÜŹĒĘųĢåÖŠ»ģÓŠĀČ»ÆĒāČÜÓŚĖ®Éś³ÉĮĖŃĪĖį”£
6”¢Ļą¶Ō·Ö×Ó×īŠ”µÄŃõ»ÆĪļ£¬Ķ¬Ź±¼ČÄÜÓė½šŹōŃõ»ÆĪļ·“Ó¦ÓÖÄÜÓė·Ē½šŹōŃõ»ÆĪļ·“Ó¦µÄŹĒĖ®
7”¢ĻąĶ¬ÖŹĮæµÄŠæ”¢Ć¾”¢Ģś”¢ĀĮ¼ÓČėµČÖŹĮ攢µČÅØ¶ČµÄŃĪĖį£Ø»ņĮņĖį£©ÖŠ£¬
£Ø£±£©ČōĖįĶźČ«·“Ó¦£¬Ōņ²śÉśĒāĘųŅ»Ńł¶ą
£Ø£²£©Čō½šŹōĶźČ«·“Ó¦”£ŌņĀĮ²śÉśĒāĘų×ī¶ą£ØĒāĘųÖŹĮ棽»ÆŗĻ¼Ū£ÆĻą¶ŌŌ×ÓÖŹĮ棩
£Ø£³£©·“Ó¦ĖŁ¶Č×īæģµÄŹĒĆ¾£¬×īĀżµÄŹĒĢś£ØæɾŻ“ĖÅŠ¶Ļ½šŹō»ī¶ÆŠŌ£©
£Ø£“£©ČōĖįĶźČ«·“Ó¦£¬ĻūŗĽšŹō×ī¶ąµÄŹĒŠæ£Ø½šŹōÖŹĮ棽Ļą¶ŌŌ×ÓÖŹĮæ£Æ»ÆŗĻ¼Ū£©
8”¢»Æѧ·ŹĮĻ£ŗŗ¬µŖĮæ×īøߵĵŖ·ŹŹĒÄņĖŲ
9”¢ÓÉĘ«¶ž¼×ėĀµÄ»ÆѧŹ½C2H8N2£¬ÄćæÉŅŌµĆµ½ÄÄŠ©ŠÅĻ¢£ŗ
¢ÅĘ«¶ž¼×ėĀŹĒŅ»ÖÖÓŠ»śĪļ””””
¢ĘĘ«¶ž¼×ėĀÓÉĢ¼”¢Ēā”¢µŖŌŖĖŲ×é³É
¢ĒŅ»øöĘ«¶ž¼×ėĀ·Ö×ÓÓÉŹ®¶žøöŌ×Ó×é³É””””
¢ČŌŚĘ«¶ž¼×ėĀÖŠĢ¼”¢Ēā”¢µŖŌ×ÓøöŹż±ČĪŖ£ŗ£±£ŗ£“£ŗ£±
¢ÉŌŚĘ«¶ž¼×ėĀÖŠĢ¼”¢Ēā”¢ŃõŌŖĖŲÖŹĮæ±ČĪŖ£ŗ£¶£ŗ£²£ŗ£·
10”¢»Æѧ·½³ĢŹ½µÄŗ¬Ņå£ŗŅŌ£²£Č£²£Ļ£½£²£Č£²”ü£«£Ļ£²”ü£ØŌŚ£½ÉĻ·½¼ÓÉĻĢõ¼žĶصē£©
¢ÅÖŹµÄŗ¬Ņå£ŗĖ®ŌŚĶصēµÄĢõ¼žĻĀÉś³ÉĮĖĒāĘųŗĶŃõĘų
¢ĘĮæµÄŗ¬Ņå£ŗ£³£¶·ŻÖŹĮæµÄĖ®ŌŚĶصēµÄĢõ¼ž·“Ӧɜ³É£“·ŻÖŹĮæµÄĒāĘųŗĶ£³£²·ŻÖŹĮæµÄŃõĘų
¢ĒĪ¢¹Ūŗ¬Ņå£ŗ£²·Ö×ÓĖ®Éś³ÉĮĖ£²·Ö×ÓµÄĒāĘųŗĶ£±·Ö×ÓµÄŃõĘų
11”¢½šøÕŹÆŗĶŹÆÄ«ĪļĄķŠŌÖŹ²»Ķ¬ŹĒŅņĪŖŌ×ÓÅÅĮŠĖ³Šņ²»Ķ¬
””””¶žŃõ»ÆĢ¼ŗĶŅ»Ńõ»ÆĢ¼»ÆѧŠŌÖŹ²»Ķ¬ŹĒŅņĪŖ·Ö×Ó¹¹³É²»Ķ¬
””””ÄĘŌ×ÓÓėÄĘĄė×Ó²»Ķ¬ŹĒŅņĪŖĶā²ćµē×ÓŹż²»Ķ¬»ņ×īĶā²ćµē×ÓŹż²»Ķ¬
””””ĖįÓė¼ī²»Ķ¬ŹĒŅņĪŖĖłŗ¬µÄĄė×Ó²»Ķ¬
””””ÉśĢśŗĶøֵIJ»Ķ¬ŹĒŅņĪŖŗ¬Ģ¼Įæ²»Ķ¬
””””ÅØĮņĖįŗĶĻ”ĮņĖį²»Ķ¬ŹĒŅņĪŖÖŹĮæ·ÖŹż²»Ķ¬
12”¢Ö¤Ć÷¶žŃõ»ÆĢ¼ÄÜÓėĖ®·“Ó¦µÄŹµŃé£ŗŹ¹×ĻÉ«ŹÆČļŹŌŅŗ±äŗģ£¬¶žŃõ»ÆĢ¼ĶØČėĖ®ÖŠ²āĘäµ¼µēŠŌ
Ö¤Ć÷¶žŃõ»ÆĢ¼ÄÜČÜÓŚĖ®£ŗ“ņæŖĘūĖ®ĘæĆ°ÅŻ£¬ÓĆĖÜĮĻĘæŹÕ¼ÆĀś¶žŃõ»ÆĢ¼ŌŁ¼ÓČėŅ»¶ØĮæµÄĖ®£¬ĖÜĮĻĘæ±ä±ń”£
13”¢°Ń½šŹō·ÅČėŃĪĖįÖŠ£¬æŖŹ¼·“Ó¦½ĻĀż£Ø±ķĆęÉśŠā£©”£×īŗóŅ²Ō½Ą“Ō½Āż£¬ŹĒŅņĪŖŃĪĖįµÄÖŹĮæ·ÖŹż±äŠ”
14”¢Ö¤Ć÷ĀČĖį¼ŲÖŠŗ¬ÓŠĀČŌŖĖŲ£ŗĀČĖį¼ŲÓė¶žŃõ»ÆĆĢ»ģŗĻ¼ÓČČ£¬ĄäČ“ŗ󽫷“Ó¦ŗóĪļÖŹČÜÓŚĖ®£¬¹żĀĖ£¬ĶłĀĖŅŗÖŠ¼ÓČėĻõĖįŅųŗĶĻ”ĻõĖį£¬ÓŠ°×É«³ĮµķÉś³É
15”¢µē½āĖ®µÄŹµŃéÖŠ£¬³£ĻņĖ®ÖŠ¼ÓČėÉŁĮæĻ”ĮņĖį»ņĒāŃõ»ÆÄĘ£¬×÷ÓĆŹĒŌöĒæĖ®µÄµ¼µēŠŌ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
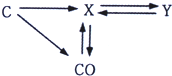 £Ø2011?ÄžµĀ£©¹¹½ØÖŖŹ¶ĶųĀēŹĒŅ»ÖÖÖŲŅŖµÄѧĻ°·½·Ø£®ĻĀĶ¼ŹĒĢ¼µ„ÖŹŗĶ²æ·ÖĢ¼µÄ»ÆŗĻĪļ¼äµÄ×Ŗ»Æ
£Ø2011?ÄžµĀ£©¹¹½ØÖŖŹ¶ĶųĀēŹĒŅ»ÖÖÖŲŅŖµÄѧĻ°·½·Ø£®ĻĀĶ¼ŹĒĢ¼µ„ÖŹŗĶ²æ·ÖĢ¼µÄ»ÆŗĻĪļ¼äµÄ×Ŗ»Æ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com