
【题目】煤、石油、天然气并称为三大化石燃料。煤的综合利用是提高燃料利用率和降低对环境污染的有效方法之一、
(一)将煤制成水煤气(主要成分是氢气和一氧化碳)就是在高温下将煤与水蒸气发生反应生成水煤气(还含有少量的水蒸气和二氧化碳)。试写出工业上生产水煤气的化学方程式_____
(二)某课题组为验证水煤气的主要成分,作了如下准备:
1.收集信息:①H2+CuO![]() Cu+H2O;②CO+CuO
Cu+H2O;②CO+CuO![]() Cu+CO2
Cu+CO2
2.设计实验装置:
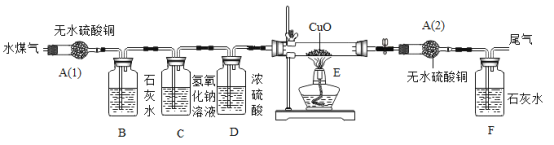
请分析上述信息和实验装置并回答下列问题:
①你认为验证水煤气中各成分的顺序依次是_____;
②装置C的目的是_____;装置D的作用是_____;
③装置E内观察到的现象是_____;
④实验中两次用到盛无水硫酸铜的装置,其目的分别是A(1)_____,A(2)_____;
⑤整个实验装置的设计有缺陷,是_____;
⑥若通入的水煤气总质量为3.2g,E中黑色粉末的质量减少了3.2g,该水煤气的有效成分的质量分数为_____。(计算结果保留1位小数)
【答案】C+H2O![]() CO+H2 水蒸气、二氧化碳、氢气、一氧化碳 除去水煤气中的二氧化碳 除去水煤气中和装置B、C中引入的水蒸气 黑色固体逐变成红色 验证水煤气中水蒸气的存在 检验水煤气中是否含有氢气 没有尾气处理装置 93.8%
CO+H2 水蒸气、二氧化碳、氢气、一氧化碳 除去水煤气中的二氧化碳 除去水煤气中和装置B、C中引入的水蒸气 黑色固体逐变成红色 验证水煤气中水蒸气的存在 检验水煤气中是否含有氢气 没有尾气处理装置 93.8%
【解析】
(一)高温下将煤与水蒸气发生反应生成水煤气(还含有少量的水蒸气和二氧化碳)化学方程式为C+H2O![]() CO+H2,故填:C+H2O
CO+H2,故填:C+H2O![]() CO+H2。
CO+H2。
(二)①水能使白色硫酸铜变蓝先通过无水硫酸铜是检验是否含有水的; 二氧化碳能使澄清石灰水变浑浊,再通过石灰水是检验是否含有二氧化碳的;再通过氢氧化钠是除去原来的二氧化碳气体,通过浓硫酸是除去原来的水蒸气,通过氧化铜是检验是否含有还原性气体,再通过无水硫酸铜,是看是否有水生成,因为氢气还原氧化铜生成铜和水所以是为了检验是否有氢气的;最后通过澄清石灰水是看有没有二氧化碳生成,因为一氧化碳还原氧化铜生成铜和二氧化碳,所以是为了检验是否含有一氧化碳的;故分别验证水煤气中各成分的顺序依次:水蒸气、二氧化碳、氢气、一氧化碳,故填:水蒸气、二氧化碳、氢气、一氧化碳。
②氢氧化钠与二氧化碳反应生成碳酸钠和水,所以氢氧化钠的目的是吸收二氧化碳,排除对一氧化碳检验的干扰;浓硫酸具有吸水性,装置D的作用是:除去水蒸气排除对氢气检验的干扰;故填:除去水煤气中的二氧化碳;除去水煤气中和装置B、C中引入的水蒸气。
③氧化铜是黑色的铜是红色的,在加热的条件下,一氧化碳和氢气能将氧化铜还原为铜,所以,装置D内观察到的现象:黑色固体变成红色;故填:黑色固体逐渐变成红色。
④实验中两次用到装置A,其目的分别是验证原混合气体中含有二氧化碳,通过验证生成物中有二氧化碳,来证明混合气体中含有一氧化碳;故填:验证原混合气体中含有二氧化碳;通过验证生成物中有二氧化碳来证明混合气体中含有一氧化碳。
⑤因为一氧化碳有毒,所以尾气一般要收集或点燃来处理,故填:没有尾气处理装置。
⑥解:生成水煤气消耗水质量![]() 生成一氧化碳质量
生成一氧化碳质量![]() 氢气质量
氢气质量![]()

设氢气还原氧化铜,固体质量减少![]() ,一氧化碳还原氧化铜固体质量减少
,一氧化碳还原氧化铜固体质量减少![]()
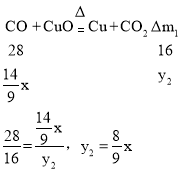

黑色粉末的质量减少了3.2g故![]() +
+![]() =3.2g,
=3.2g,![]() =1.8g,
=1.8g,
![]() =2.8g,
=2.8g, ![]() =0.2g
=0.2g
故有效成分质量分数:
![]()
故填:93.8%


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:初中化学 来源: 题型:
【题目】小颖同学将铁粉投入硫酸铜溶液中时,发现生成红色固体的同时有较多的气泡放出,小颖对产生气泡的现象提出疑问,邀请兴趣小组的同学们展开了如下探究实验。
(提出问题)产生的气体是什么呢?
(作出猜想)兴趣小组的同学分别作出了如下猜想:小军的猜想:O2;小红的猜想:SO2;小颖的猜想:H2;小伟的猜想:N2。
(交流讨论)同学们经过讨论一致认为小伟的猜想不正确,依据是_____。
(查阅资料)SO2具有刺激性气味,易溶于水,能与NaOH溶液发生反应生成Na2SO3和水。
(实验探究)同学们收集气体,并分别对各自的猜想进行验证。
实验操作 | 实验现象 | 实验结论 | |
小军 | 将带火星的木条伸入到收集的气体中 | _____ | 猜想不正确 |
小红 | 将产生的气体通入盛有NaOH溶液的洗气瓶中,称量质量 | 通气前后洗气瓶的质量不变 | 猜想_____(填“正确”或“不正确”) |
小颖 | 将产生的气体用尖嘴玻璃管导出后点燃,并用冷而干燥的烧杯罩在火焰的上方 | 气体燃烧,产生淡蓝色火焰,烧杯内壁_____ | 猜想正确 |
写出小颖实验中发生反应的化学方程式_____。
(评价与改进)
(1)小红认为小军和小颖的实验方案都存在安全隐患,理由是_____。
(2)实验结束后,老师认为不需要进行实验即可通过更简便的方法验证小红的猜想,你认为所选择更为简便方法的依据是_____。
(拓展与延伸)
(1)由实验探究推测,可知硫酸铜溶液中可能含有呈酸性的物质,一般不用紫色石蕊溶液检验硫酸铜溶液酸碱性的原因是_____。
(2)据老师介绍,CuSO4可做催化剂,能加快过氧化氢的分解速率。为了验证老师的说法,需要进行的探究内容有:①是否能加快过氧化氢的分解;②_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知镉(Cd)的金属活动性与铁、锌相近,镉元素在化合物中常显+2价.
(1)将镉丝插入下列溶液有明显现象的是______(填序号).
①NaCl溶液 ②HCl溶液 ③AgNO3溶液 ④NaOH溶液
(2)镍镉电池应用广泛,为了防止污染环境,从废旧镍镉电池中回收镉的一种方法如下:
步骤1:将废旧电池破碎成细颗粒后焙烧,将镉转化为氧化镉(CdO);
步骤2:将含氧化镉的细颗粒和炭粉混合后,隔绝空气加热至1200℃,可得镉蒸气和一氧化碳.
步骤2中氧化镉变成镉的化学方程式是______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有三组固体混合物:
①Na![]() O
O![]() (过氧化钠)和NaOH的混合物,其中Na的质量分数是58% ;
(过氧化钠)和NaOH的混合物,其中Na的质量分数是58% ;
②FeSO![]() 和Fe
和Fe![]() (SO
(SO![]() )
)![]() 的混合物,其中Fe的质量分数是31%;
的混合物,其中Fe的质量分数是31%;
③Na![]() S Na
S Na![]() SO
SO![]() ,和Na
,和Na![]() SO
SO![]() 的混合物,其中S的质量分数是25.6%。
的混合物,其中S的质量分数是25.6%。
其中含氧元素的质量分数最高的一组是___为__%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是化学学习的重要工具,下图是元素周期表的一部分,请认真观察分析并回答问题:
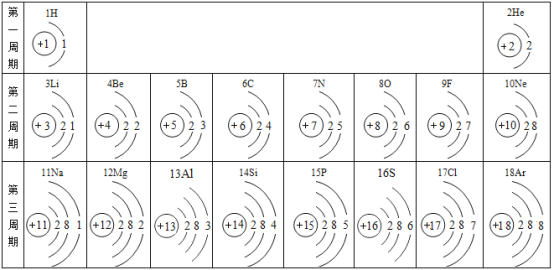
(1)元素周期表中的各种元素的本质区别是_____;决定元素化学性质的是_____
(2)决定元素所在的周期数的是_____第二周期元素的原子核外电子排布的规律是_____。
(3)F、Cl、S三种非金属元素的原子得电子能力逐渐增强,根据这三种非金属元素的原子结构推测:非金属元素的原子得电子能力的强弱主要与_____有关。
(4)水(H2O)、双氧水(H2O2)、重水(D2O,“D”表示原子核中有一个质子和一个中子的氢原子)三种物质,从物质组成的角度看,这三种物质所含的元素共有_____种,从化学性质的角度看,_____与水的化学性质有较大的差异。
(5)原子通过得失电子后可形成稳定粒子。核外有10个电子的粒子有:
①阳离子:_____;
②阴离子:_____;
③中性粒子:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂车间以MnO2为原料制备高纯MnCO3的流程如下。下列说法正确的是( )
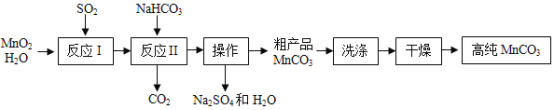
已知:①反应I的化学方程式:MnO2+SO2=MnSO4;
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100°C时开始分解。
A.反应I中只有Mn元素的化合价发生了改变
B.反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有Mn(OH)2
C.为快速获得高纯MnCO3,需选择干燥的条件是高于100°C
D.若原料MnO2有8.7kg,假设其它原料都足量,实验过程无损失,最终得到的产品中含11.5kgMnCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:Na2CO3+H2O+CO2=2NaHCO3。将二氧化碳气体缓缓通入到一定质量的Na2CO3溶液中,测得变量y随时间的变化趋势如图所示。变量y可表示的是
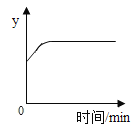
A.溶剂的质量B.溶液中碳元素的质量
C.碳酸钠的质量分数D.溶液中钠元素的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是几种粒子的结构示意图:
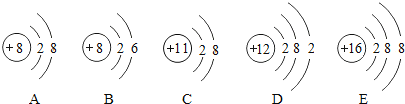
(1)A~E共有_____种元素,B所表示的元素位于元素周期表的第_____周期,该元素的原子容易_______(填“得到”或“失去”)电子。
(2)表示原子的粒子有_____(填序号,下同);
(3)表示阴离子的有____;
(4)表示阳离子的有_____________;
(5)表示相对稳定结构的是_________;
(6)在化学反应中易得到电子的粒子是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2015年12月南昌地铁1号线正式通车。请回答下列问题:
(1)在制造车体时要使用大量塑料,塑料属于_____(填“金属材料”或“有机合成材料”);
(2)地铁列车使用铝合金作车体材料,主要利用其_____;
A密度小硬度大 B强度髙密度大 C导电性好 D熔点高
(3)工业上常用氧化铝在一定条件下电解生成金属铝和氧气,反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com