
(1)为测定空气中氧气的含量,小华同学设计了如图15甲所示的实验方案:在一个隔热效果良好的容器上方安装一个可自由上下移动的活塞(活塞质量忽略不计,起始位置在5刻度处)。加热容器,使白磷燃烧。待反应完全,容器冷却至室温后,活塞最后停在刻度 处。有位同学用木炭取代白磷来进行实验,结果实验失败,请你分析实验失败的原因是 。
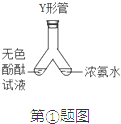
(2)为证明CO2能与NaOH溶液反应,小明同学设计了如图15乙所示的实验方案:从左端导管处通入CO2气体,若观察到____________________________的现象,证明CO2与NaOH溶液发生了反应。小军同学认为也可通过向CO2与NaOH溶液反应的生成物中加入一种试剂的方法来证明,他加入的这种试剂可能是____________。
 作业辅导系列答案
作业辅导系列答案科目:初中化学 来源: 题型:阅读理解
| ||
| ||

| 9(m-n) |
| 2w |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
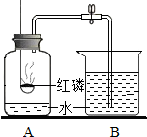 (2012?哈尔滨模拟)如图为某同学设计的测定空气中氧气含量的实验:
(2012?哈尔滨模拟)如图为某同学设计的测定空气中氧气含量的实验:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 1 |
| 5 |

| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源:化学教研室 题型:059
对空气有关问题的探究
没有空气就没有生命,也就没有生机勃勃的地球.请你参与下列问题的讨论.
(1)
空气属于________(填“混合”或“纯净”)物.如果空气中没有________,大自然中就会失去雨、雪、雾、霜、露等自然现象.超市出售的一些袋装食品内常充有防腐的气体,它来自于空气,请你分析这种气体可能是空气中的________.(2)
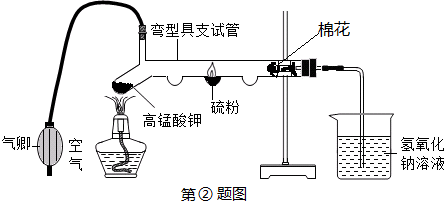
二氧化硫( )、悬浮颗粒物、氮氧化合物是主要的大气污染物.某校化学课外活动小组为测定校园附近空气中二氧化硫(
)、悬浮颗粒物、氮氧化合物是主要的大气污染物.某校化学课外活动小组为测定校园附近空气中二氧化硫( )、悬浮颗粒物的含量,根据反应原理,设计如图所示装置.
)、悬浮颗粒物的含量,根据反应原理,设计如图所示装置.


①空气流量表能测出经过的空气质量,测定二氧化硫
( )、悬浮颗粒物含量时,装置的连接顺序是________.
)、悬浮颗粒物含量时,装置的连接顺序是________.
②为准确测定:二氧化硫
( )的含量,实验时当观察到A中________时.应立即关闭抽气泵.
)的含量,实验时当观察到A中________时.应立即关闭抽气泵.
③为测定空气中悬浮颗粒的含量,除要测出抽人空气的质量外,还要测
________(填序号).|
A .实验前A的质量 |
B .实验后A的质量 |
|
C .实验前C的质量 |
D .实验后C的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
化学是一门以实验为基础的科学。根据下图所示实验,回答以下问题。




A B C D
① A为测定空气中氧气含量的实验装置,有关反应的化学方程式为 (1) ,通过该实验可得出氧气约占空气总体积的 (2) 的结论。
② 集气瓶B中的现象是铁丝在氧气中剧烈燃烧, (3) ,放出大量的热,有黑色固体生成。该反应的化学方程式为 (4) 。
③ 1800年,英国化学家尼科尔森通过电解水得到了氢气和氧气。图C是水的电解装置,反应化学方程式为 (5) 。,实验证明了水是由 (6) 氢、氧两种元素
组成的化合物。
④ 用坩埚钳夹住已擦亮的镁条,放在酒精灯上点燃后,立即伸进盛有二氧化碳集气瓶中(图D),发现镁条剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体,该反应中生成白色固体是 (7) ,本实验使你对燃烧条件产生的新认识是 (8) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com