我国规定饮用水的硬义不能超过25度.硬度的表示方法是:将水中的Ca2+和Mg2+都看成Ca2+,并将其折算成CaO的质量.通常把1L水中含有10 mgCaO称为1度,1L水中含有20mgCaO即为2度;依此类推.8度以上为硬水,8度以下为软水.
(1)自然界的水中都溶有一定量的Ca(HCO3)2和Mg(HCO3)2,它们在受热时分别分解成CaCO3和Mg(OH)2,这两种白色固体在容器内壁上积淀,即形成水垢.请用化学方程式表示除去锅炉或水壶里水垢的原理.______、______.
(2)在日常生活中,如何用简便的方法确定某水样是硬水还是软水(写出主要操作、现象、结论)?______.
(3)取某水样10mL,经实验测定,其中含Ca2+0.001g,含Mg2+0.00048g,试通过计算回答:该水样从硬度角度看,是否符合饮用水标准?(写出计算过程)
______.
解:(1)由于碳酸钙、氢氧化镁都能与酸反应,可用稀盐酸除去.化学方程式为CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑
Mg(OH)
2+2HCl=MgCl
2+2H
2O;
(2)确定硬度有很大差异的硬水和软水的方法:取等体积的样品,都加入相同量的肥皂水,一起振荡,产生的泡沫较少、浮渣较多的是硬水.
(3)10mL水中,含Ca
2+0.001g,含Mg
2+0.00048g
则1L水中含Ca
2+100mg,Mg
2+48mg.将Mg
2+48mg折合成Ca
2+的质量为80mg,可看成1L水中共含Ca
2+180mg,由钙离子可求出氧化钙的质量为:
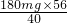
=252mg;则水样的硬度为252mg/10mL=25.2度>25度,不符合饮用水标准.
故答案为:①CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;Mg(OH)
2+2HCl=MgCl
2+2H
2O;
(2)取等体积的样品,都加入相同量的肥皂水,一起振荡,产生的泡沫较少、浮渣较多的是硬水,
(3)不符合饮用水标准.
分析:(1)碳酸钙、氢氧化镁都能与酸反应;
(2)肥皂水可以用来鉴别硬水和软水;
(3)根据钙离子的质量可以计算出水样的硬度.
点评:本题考查硬水和软水的检验、新信息处理能力及碳酸盐的检验方法,解题的关键是掌握检验方法和对新信息处理能力.

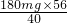 =252mg;则水样的硬度为252mg/10mL=25.2度>25度,不符合饮用水标准.
=252mg;则水样的硬度为252mg/10mL=25.2度>25度,不符合饮用水标准.
