
甲、乙、丙、丁四位同学用锌与稀硫酸反应,所得相关数据记录如下表
(实验中的误差忽略不计).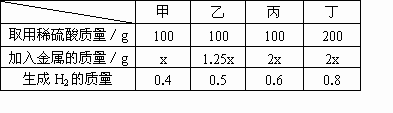
计算:
(1)甲同学加入金属锌的质量x.(2)稀硫酸中溶质的质量分数.
|
根据质量守恒,甲、乙、丙等质量的酸随着锌质量的增加,产生 H2的质量也增加,证明甲、乙中金属完全反应;丁、丙中等质量的金属随酸质量的增加,产生H2的质量也增加,因此丙中的2x g金属过量,酸完全反应;而丁产生H2的质量并未随酸量增加一倍而等倍数增加,说明金属已完全反应,求x时可用甲、乙、丁任何一组数据,求H2SO4时应用丙的数据.(1)设甲加入Zn的质量为x Zn+H2SO4=ZnSO4+H2↑ 65 2 x 0.4g x= (2)设稀硫酸中溶质的质量分数为y% Zn+H2SO4=ZnSO4+H2↑ 98 2 100g·y% 0.6g y%= |


 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:初中化学 来源: 题型:
| ||
| A、甲同学说:磷、氧气、五氧化二磷三种物质的质量比为4:5:2 |
| B、乙同学说:这是一个分解反应 |
| C、丙同学说:生成物是一种混合物 |
| D、丁同学说:反应后固体的质量有所增加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com